«Каналы жизни»: новые подходы к лечению сердечно-сосудистых заболеваний
В последние годы в научной литературе много внимания уделяют результатам исследований ионных каналов, которые, как полагают ученые, являются ключом к созданию принципиально новых технологий терапии многих заболеваний. О некоторых особенностях этих каналов и перспективах таких исследований рассказывает Анатолий Соловьев, д-р мед. наук, профессор, зав. отделом экспериментальной терапии и руководитель Межведомственной лаборатории доклинического изучения лекарственных средств ГУ «Институт фармакологии и токсикологии НАМН Украины»
— Анатолий Иванович, каково предназначение ионных каналов в клетке?

Анатолий Соловьев
— Ионные каналы клеточной мембраны имеют огромное значение для жизни клеток. Они обеспечивают обмен клетки с окружающей средой веществом, энергией и информацией, с них начинаются и ими поддерживаются процессы возбуждения и торможения в нервной системе и мышцах, именно они (вместе с другими молекулярными рецепторами) обеспечивают восприятие клеткой внешних сигналов. С помощью ионных каналов происходит передача в клетку управляющих сигналов из окружающей ее среды. Именно ионные каналы обеспечивают синаптическую передачу возбуждения от возбужденного нейрона на другие клетки. Обобщая, можно сказать, что почти все важнейшие физиологические процессы в организме начинаются с ионных каналов и поддерживаются ими. Их смело можно назвать «каналами жизни».
— Что же лежит в основе работы таких каналов?
— Потенциал-управляемые натриевые каналы — ключевой элемент нервной системы животных и человека. Когда нейрон находится в состоянии покоя, на его мембране (представляющей собой, при определенном упрощении, конденсатор) благодаря работе специальных систем — ионных насосов, поддерживается определенный электрический потенциал. В это время натриевые каналы закрыты. Когда же происходит деполяризация мембраны, они реагируют на снижение мембранного потенциала и открываются (отсюда название «потенциал-управляемые»; бывают и другие каналы, например лиганд-управляемые, которые открываются или закрываются в ответ на присоединение определенной молекулы, например, ацетилхолина). Ионы Na+ текут внутрь клетки, перенося положительный заряд с внешней стороны на внутреннюю, в результатае чего потенциал покоя сменяется потенциалом действия.
Потенциал-управляемые натриевые каналы гомологичны, т.е имеют общую принципиальную структуру, хотя и разную специализацию, ряду других каналов — прежде всего, потенциал-управляемым калиевым и кальциевым каналам. Различаются они главным образом конструкцией «селективного фильтра» — узкого участка поры, где на основе тонких молекулярных взаимодействий происходит отбор ионов, для которых канал проницаем.
По результатам рентгеноструктурного анализа каналов бактерий первые детальные сведения об устройстве калиевых каналов были опубликованы лишь в 1998 г. Родериком Маккинноном (США), который стал лауреатом Нобелевской премии по химии всего через пять лет, в 2003 г., настолько очевидным было для научного сообщества значение этих результатов.
— С помощью каких методов изучают свойства таких непростых микрообъектов?
— Для исследования ионных каналов необходимы совершенно уникальные методики. Одним из первых создателей таких методик был мой учитель, академик Платон Григорьевич Костюк — ученик лауреата Нобелевской премии Дж.К. Экклса и крупнейший специалист в области нейрофизиологии. Еще в 50-е годы прошлого столетия он опубликовал книгу «Микроэлектродная техника», которая была удостоена премии им. И.П. Павлова АН СССР, где были изложены основы подобных методик, разработанных в том числе и лично автором. Ныне одним из наиболее информативных методов исследования ионных каналов является метод локальной фиксации потенциала, так называемый пэтч-клэмп метод, заключающийся в том, что фрагмент клеточной мембраны изолируют с помощью специальной микропипетки. Эта методика позволяет контролировать разность потенциалов между сторонами мембраны, а также помещать ее в среду с определенным химическим составом. В этих хорошо контролируемых условиях измеряют ионные токи, проходящие через мембрану, и делают вывод о том, как ионные каналы реагируют на электрическое и химическое воздействие. Метод настолько чувствителен, что позволяет наблюдать прохождение тока через одиночный ионный канал, поведение и химические превращения единичных молекул, взаимодействующих с мембраной. Немецкие исследователи Эрвин Неер и Берт Сакман, разработавшие эту методику, и, кстати, многому научившиеся в Институте физиологии им. А.А. Богомольца в Киеве, получили в 1991 г. Нобелевскую премию.
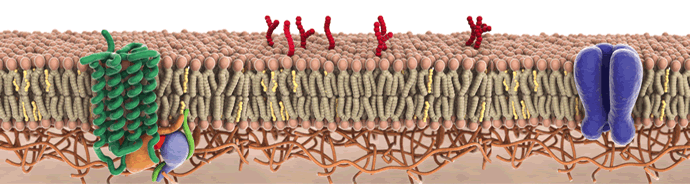
Cтруктура клеточной мембраны: видны трансмембранные белки, образующие каналы (синий, зеленый цвет), на поверхности – гликолипиды (красный цвет)
— Что может вызвать аномалии в работе ионных каналов и к чему это может привести?
— Болезни, вызванные нарушением функции субъединиц ионного канала или белков, регулирующих их деятельность, называют каналопатиями. Они могут быть врожденными (вследствие мутации генов, кодирующих канал) или приобретенными, как, например, в результате аутоиммунной атаки на канал или воздействия токсиканта.
В последние годы некоторые разновидности сердечных тахиаритмий были отнесены к генетическим нарушениям в каналах, которые управляют ионными потоками через мембраны клеток сердца. Такие каналопатии — аномально функционирующие каналы вследствие врожденных мутаций — могут поразить любую электрически активную клетку и не ограничиваются только сердцем. Так, некоторые виды мигрени, эпилепсии, периодического паралича и заболеваний мышечной ткани, по-видимому, обусловлены каналопатией.
— А такой фактор, как ионизирующая радиация, может прямо или косвенно влиять на работу ионных каналов?
— Сейчас мы уже твердо знаем, что одной из основных мишеней для действия ионизирующего излучения являются сосуды и прежде всего их внутренняя выстилка, эндотелий. В результате воздействия ионизирующего излучения среди ликвидаторов Чернобыльской катастрофы широкое распространение получили заболевания сердечно-сосудистой системы, в частности, нарушения коронарного кровообращения и артериальная гипертензия. Кроме этого добавилось снижение чувствительности их сосудов к стандартным вазодилататорам, например, нитроглицерину. Это побудило нас приступить к изучению клеточных механизмов действия радиации на эффекторные элементы сосудистой стенки, исследовать пусковые факторы артериальной гипертензии и сосудистых дисфункций, индуцированных ионизирующей радиацией.
— И какие же были получены результаты?
— Было установлено, что калиевые каналы плазматической мембраны гладкомышечных (ГМК) и эндотелиальных клеток (ЭК) сосудов, одним из основных подтипов которых являются так называемые Са2+-зависимые калиевые каналы большой проводимости (BKCa), играют определяющую роль в регуляции мембранного потенциала и, следовательно, уровня изометрического напряжения ГМК в условиях действия ионизирующей радиации, то есть именно они и выступают основной мишенью ее действия в сосудистой стенке. Облучение экспериментальных крыс в нефатальных дозах приводит к подавлению токов через ВКСа в ГМК и ЭК, снижению амплитуды эндотелийзависимого расслабления и увеличению реакции сосудов в ответ на действие агонистов α-адренорецепторов. Все эти факторы вместе взятые обусловливают значительное повышение артериального давления.
— Какие, на Ваш взгляд, перспективы в борьбе с таким явлением?
— Открытие явления РНК-интерференции ознаменовало появление перспектив в создании принципиально новых подходов к лечению ангиопатий различного генеза и артериальной гипертензии. Появился эффективный механизм для избирательного торможения экспрессии заданного гена на стадиях его трансляции или транскрипции.
Данная технология является одной из высокоспецифичных современных методов целевой генотерапии, суть которого состоит в угнетении экспрессии определенного гена на стадии трансляции или в нарушении его транскрипции (посттранскрипционный сайленсинг). Проведенные нами эксперименты подтвердили возможность использования феномена РНК-интерференции для устранения сосудистых нарушений, вызванных воздействием радиации, при экспериментальном сахарном диабете и эссенциальной артериальной гипертензии путем воздействия на гены, кодирующие экспрессию или самих BKCa, или же генов, кодирующих экспрессию регуляторных ферментов, таких как протеинкиназа С.
— Существуют ли еще какие-либо методы воздействия на работу ионных каналов, позволяющие надеяться на их эффективное использование в будущем в медицинской практике?
— Мы также провели эксперименты по выяснению возможности использования стволовых клеток человека для лечения сосудистой патологии. Взрослые мезенхимальные стволовые клетки человека были протестированы на экспериментальных крысах с артериальной гипертензией, индуцированной воздействием ионизирующего облучения, и на крысах с генетически детерминированной артериальной гипертензией. Оказалось, что однократное введение таким животным стволовых клеток приводило к нормализации нарушенного эндотелийзависимого расслабления сосудов и восстановлению функции BKCa в ГМК.
Интересные исследования были проведены нами и по использованию явления плазменного резонанса на поверхности наночастиц золота для управления ионными каналами путем воздействия на их потенциал-чувствительный сенсор. Этот метод пока еще является довольно экзотическим способом дистанционного контроля ионных каналов и находится в стадии экспериментальной разработки. Тем не менее нам удалось получить убедительные данные, свидетельствующие, что плазменные наночастицы золота обладают способностью открывать калиевые каналы в плазматической мембране клеток, не образуя с ними каких-либо химических связей. Это происходит посредством взаимодействия электронного облака на поверхности наночастиц с сенсором напряжения канала, причем этот эффект усиливается при облучении клетки лазером определенной длины волны за счет явления плазменного резонанса.
Таким образом, только фундаментальные исследования ионных каналов могут дать реальную надежду на прорыв в данной области, что позволит создать принципиально новые подходы к лечению пациентов не только с нарушениями коронарного кровообращения и артериальной гипертензией, но и с другими заболеваниями.
Подготовил Руслан Примак, канд. хим. наук
Фото на слайдере: фрагмент клеточной мембраны; видны выступающие над поверхностью мембраны гликолипиды (на переднем плане) и трансмембранные белки; компьютерная 3-D модель
“Фармацевт Практик” #02′ 2015
