Внутрибольничные инфекции: особенности, источники, возбудители
Ежегодно в США регистрируют около 1,7 млн случаев внутрибольничных инфекций, вызванных микроорганизмами, при этом 99 тыс. из них заканчиваются летально. В развитых странах Европы смертность от внутрибольничных инфекций составляет 25 тыс. случаев в год, из них две трети обусловлены грамотрицательными бактериями. В нашей стране внутрибольничные инфекции в два раза повышают риск летального исхода
Внутрибольничные инфекции
Изучение внутрибольничных инфекций (ВБИ) началось более 150 лет назад, но по-прежнему они остаются серьезной проблемой, приводя к удлинению сроков лечения, хронизации процесса, инвалидности, а в наиболее тяжелых случаях — к смерти больных. Согласно определению ВОЗ, внутрибольничными инфекциями считаются любые клинически выраженные заболевания микробного происхождения, поражающие больного в результате его госпитализации или посещения лечебного учреждения либо возникающие в течение 30 дней после выписки из больницы.
К внутрибольничным инфекциям также относятся инфицирование сотрудников больницы, связанное с их профессиональной деятельностью. Эти болезни отличаются механизмами и факторами передачи, особенностями течения эпидемиологического и инфекционного процессов, а также особой ролью медицинского персонала в возникновении, поддержании и распространении инфекции. Подобные инфекции могут быть обусловлены широким внедрением в практику инструментальных, эндоскопических, биохимических и других методов диагностики, которые сопряжены с нарушением целости покровов тела человека. Проблема в том, что конструкция некоторых медицинских приборов не позволяет произвести их полную стерилизацию после каждой процедуры, оставляя лазейку для проникновения нежелательных микробов во внутреннюю среду организма человека.
Агенты ВБИ
Всего насчитывается более 200 агентов, которые могут быть причиной внутрибольничных инфекций. До появления антибиотиков основными из них были стрептококки и анаэробные палочки. Однако после начала клинического применения антибиотиков возбудителями основных внутрибольничных инфекций стали ранее непатогенные или условно-патогенные микроорганизмы. К ним относятся стафилококки (Staphylococcus aureus, St. epidermidis, St. saprophiticus), стрептококки (Streptococcus spp.), энтерококки (Enterococcus faecalis, Enterococcus durans), эшерихия (Escherichia coli), клебсиелла (Klebsiella spp.), энтеробактер (Enterobacter spp.), протей (Proteus mirabilis), серрация (Serratia marcescens), псевдомонада (Pseudomonas aeruginosa). Нередко встречаются ВБИ, вызываемые Providencia spp., Stenotrophomona smaltophilia, Acinetobacter baumannii, Citrobacter spp., Clostridium difficile и другими микроорганизмами.
Всего насчитывается более 200 агентов, которые могут быть причиной внутрибольничных инфекций
Очень опасна комбинация «стафилококк+протей+синегнойная палочка», поскольку в результате развивается особо тяжелый деструктивно-некротический энтероколит с парезом кишечника и симптомами его динамической непроходимости, следствием которых нередко является летальный исход.
Роль облигатно-патогенных микроорганизмов в развитии внутрибольничных инфекций невелика. В неинфекционных стационарах регистрируют несколько нозологических форм инфекций, вызванных возбудителями этой группы. К ним относятся вирусы гепатитов В, С, D, ВИЧ, гриппа и других ОРВИ, острых кишечных вирусных инфекций, герпеса, цитомегаловирусной инфекции, а также анаэробные клостридии и хламидии.
Читайте также: Смогут ли антимикробные пептиды заменить антибиотики?
ВОЗ предупреждает
Эксперты ВОЗ совместно с отделом инфекционных заболеваний при Тюбингенском университете (Германия) назвали 12 бактерий, которые представляют наибольшую опасность для здоровья человека.
В первую критическую группу вошли Acinetobacter baumannii, Pseudomona saeruginosa и Enterobacteriaceae, которые часто выявляют в больницах и домах престарелых, причем заражение ими может привести к развитию смертельных инфекций, например пневмонии и заболеваний крови. Эти бактерии устойчивы к большинству антибиотиков, в том числе карбапенемам и цефалоспоринам.
Основные пути приспособления больничных штаммов — это устойчивость к одному или нескольким антибиотикам широкого спектра действия и снижение чувствительности к антисептикам
Во вторую группу списка ВОЗ включены Enterococcus faecium, Staphylococcus aureus, Helicobacter pylori, Campylobacter spp., Salmonellae и Neisseria gonorrhoeae. К третьей категории отнесены Streptococcus pneumoniae, Haemophilus influenzae и Shigella spp.
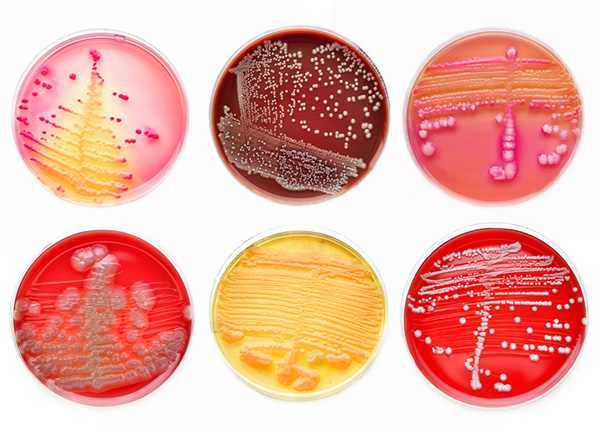
Госпитальные штаммы
В результате циркуляции условно-патогенных микроорганизмов в больнице происходит их естественный отбор с образованием наиболее устойчивого госпитального штамма. Мутации или горизонтальный перенос генов с помощью плазмид позволяет больничным микроорганизмам приобрести новые свойства, не характерные для «диких» штаммов этого вида.
Основные пути приспособления больничных штаммов — это устойчивость к одному или нескольким антибиотикам широкого спектра действия и снижение чувствительности к антисептикам. Госпитальные штаммы очень разнообразны, в каждой больнице или отделении возможно появление своего характерного штамма со свойственным только ему набором биологических свойств. При этом популяции возбудителей внутрибольничных инфекций отличаются не только гетерогенностью, но и динамичностью во времени.
Из больниц антибиотикорезистентные штаммы, особенно это касается грамотрицательных бактерий, постепенно начинают распространяться во внебольничную среду.
Читайте также: Биопленки — еще одна причина неэффективности антибиотиков
Эковары
Эковары — это варианты одного вида микроорганизма, которые приспособились к обитанию в определенной экосистеме. В данном случае выделяют больничные и внебольничные эковары. Больничными эковарами люди заражаются в основном во время инъекций, операций, переливания крови, гемосорбции, гемодиализа, мануальных и эндоскопических исследований и др.
Госпитальные инфекции, обусловленные внебольничными эковарами, часто возникают при нарушении целости покровов тела на фоне общего снижения иммунитета. Возбудители инфекций проникают во внутреннюю среду организма при повреждении слизистых оболочек, через ожоги, травматические раны, открытые гнойно-воспалительные очаги.
Устойчивые к большинству антибиотиков штаммы золотистого стафилококка (methicillinresistant Staphylococcus aureus — MRSA) стали настоящим бичом больниц. Несмотря на все усилия, ликвидировать инфекцию не удается
Больничные эковары способны вызывать госпитальную инфекцию не только при снижении функции иммунной системы, но и при нормальном иммунном ответе после инъекций или операций. Причем инфицирующая доза больничного эковара может быть относительно небольшой. Для появления инфекции, вызванной внебольничным эковаром, кроме снижения иммунитета, необходимо еще два условия: пассивное проникновение возбудителя во внешнюю среду организма и массивная инфицирующая доза.
Генетическая стабильность больничных инфекций Pseudomonas aeruginosa
Прежде считалось, что в больничной среде бактерии изменяются ускоренными темпами, увеличивая таким образом генетическое разнообразие внутрибольничной микрофлоры. Для изучения этого вопроса датские ученые проследили генетические изменения бактерии Pseudomonas aeruginosa, которые произошли с 70-х годов прошлого века в пределах одной из больниц Копенгагена. Для этого они использовали бактериальные штаммы, выделенные в анализах больных муковисцидозом, поскольку Pseudomonas aeruginosa является источником инфекций дыхательных путей, осложняя течение этой болезни.
Хирург и специалист по инфекционным заболеваниям Марк Шпигельман из Университетского колледжа в Лондоне считает, что повышенные требования к гигиене в хирургических клиниках парадоксальным образом способствуют распространению внутрибольничных инфекций
Один вариант штамма в течение 35 лет дал около 200 000 поколений, переходя от одного пациента к другому. В связи с высокой неоднородностью условий и длительным временем можно было бы ожидать широкой генетической диверсификации исходного штамма, но оказалось, что внутрибольничные инфекционные возбудители после периода быстрых адаптаций изменяются относительно мало, скорость мутирования у них низкая и расщепления на отдельные линии не происходит.
Читайте также: 10 перспективных альтернатив антибиотикам
Эти наблюдения на первый взгляд кажутся противоречивыми, так как долгая эволюция в нестабильных условиях могла бы способствовать повышению генетического разнообразия. Тем не менее выяснилось, что, несмотря на то что внутренняя среда больного весьма неустойчива и разнородна из-за инфекций и постоянного лечения всевозможными препаратами, эта разнородность не способствует быстрому увеличению генетического разнообразия.
Clostridium difficile
Спорообразующая бактерия Clostridium difficile относится к стойким и трудноискоренимым возбудителям больничных инфекций. Заражение происходит через руки медицинского персонала, например, при измерении ректальной температуры, причем не помогает даже использование индивидуальных чехлов для датчиков.
У получавших антибиотики больных (даже однократно перед операцией) под влиянием токсинов Clostridium difficile возможно развитие псевдомембранозного колита, основным проявлением которого является диарея. У некоторых больных профузная диарея сопровождается интоксикацией, высокой лихорадкой, лейкоцитозом. Если пациент продолжает получать антибиотики вплоть до выписки, то псевдомембранозный колит может начаться дома.
MRSA — повод для изменений правил больничной гигиены
Устойчивые к большинству антибиотиков штаммы золотистого стафилококка (methicillinresistant Staphylococcus aureus — MRSA) стали настоящим бичом больниц. Несмотря на все усилия, ликвидировать инфекцию не удается. Вне больниц бактерия, как правило, теряет активность. Однако в последнее время все чаще отмечают случаи, когда инфекция выходит за пределы медицинских учреждений.
Хирург и специалист по инфекционным заболеваниям Марк Шпигельман из Университетского колледжа в Лондоне считает, что повышенные требования к гигиене в хирургических клиниках парадоксальным образом способствуют распространению внутрибольничных инфекций. При этом он указывает на два принципиальных факта, которые должны объяснить неэффективность борьбы с инфекцией в больницах. Во-первых, избыточные меры гигиены, применяемые в больницах, особенно в хирургических отделениях, уничтожают безвредные бактерии, создавая тем самым среду для заселения бактериями MRSA. Во-вторых, применение антибиотиков с гигиенической целью, в частности использование антибактериального мыла, не только приводит к появлению устойчивых к антибиотикам штаммов, но и активизирует защитные механизмы у бактерий, которые в менее агрессивной среде не действуют.
Читайте также: «Пожиратели бактерий» возвращаются, или Чем нам могут быть полезны бактериофаги?
Как специалист по истории и развитию инфекционных заболеваний в древних человеческих популяциях Марк Шпигельман предлагает предпринять ряд мер по борьбе с инфекцией. Прежде всего надо строго разделить больницы, где используют антибиотики, от тех, где их не применяют (прежде всего это касается хирургических отделений). Разделение должно быть очень жестким. Персонал не должен совмещать работу в больницах разного типа.
В случае необходимости использовать антибиотики в клинике, где они запрещены, больного следует перевести в другое медицинское учреждение. Кроме того, выдвинуто неожиданное предложение по изменению гигиенических процедур. Предлагается вместо антибиотиков при подготовке к операции использовать пробиотики, которые помогут противостоять болезнетворным бактериям.
Татьяна Кривомаз, д-р техн. наук, канд. биол. наук, профессор
“Фармацевт Практик” #6′ 2018