Почему клеточные «водопроводы» так интересны фармакологам?
В последнее время у фармакологов всего мира огромный интерес вызывают не только ионные каналы, но и их ближайшие «родственники» — трансмембранные каналы, обеспечивающие быстрый транспорт воды через биологические мембраны, и образующие трансмембранные белки, получившие название «аквапорины». О том, чем вызван интерес к этим каналам, рассказывает Анатолий Соловьев, д-р мед. наук, профессор, зав. отделом экспериментальной терапии, руководитель Межведомственной лаборатории доклинического изучения лекарственных средств ГУ «Институт фармакологии и токсикологии НАМН Украины», дважды лауреат Государственной премии Украины
— Анатолий Иванович, какова предыстория открытия аквапоринов?
— Как ни банально это звучит, но основой жизни является вода, которая составляет примерно 70% массы большинства живых организмов. Однако ее содержание внутри и вне клетки различается, вследствие чего клетка вынуждена строго регулировать поступление этого «универсального» растворителя. Оказывается, регуляция водного баланса внутри клеток влияет на их способность выполнять специфическую, жизненно необходимую для всего организма функцию. Регулируя поступление воды и тем самым свой объем, нервные клетки, например,  влияют на состояние собственных ионных каналов, генерирующих нервные импульсы.
влияют на состояние собственных ионных каналов, генерирующих нервные импульсы.
Концентрация солей, жиров, белков и углеводов внутри клетки обычно превышает таковую снаружи, а это значит, что относительное количество воды в ней меньше, чем в тканевых жидкостях. Клетка испытывает постоянное давление воды, которому должна сопротивляться в течение всей жизни.
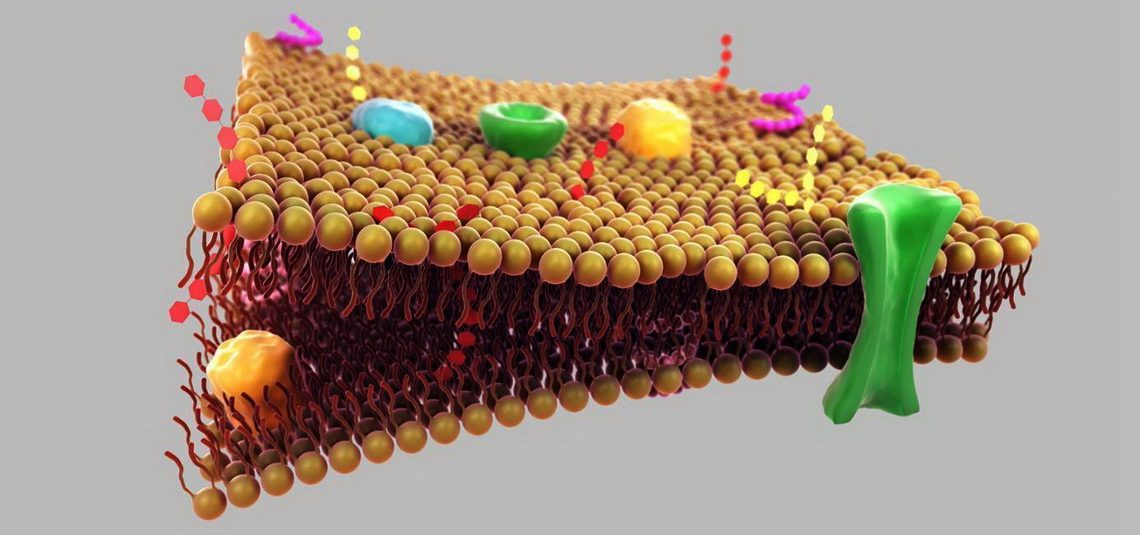
Исследователям давно стало ясно, что вода не может преодолевать клеточную мембрану только путем диффузии, поскольку скорость и интенсивность такого водообмена явно недостаточны. Было высказано предположение, что, по-видимому, для быстрого транспорта воды в клетке существуют специальные мембранные каналы с особым механизмом регуляции водных потоков, который к тому же должен быть очень специфичным, чтобы вместе с молекулой воды не проникали вредные водорастворимые (гидрофильные) соединения, способные повредить ДНК и клеточные белки либо блокировать внутриклеточные реакции. Наличие этого механизма было обнаружено у специальных трансмембранных каналов, обеспечивающих быстрый транспорт воды через биологические мембраны.
В 2003 г. молекулярный биолог Питер Эгр и биохимик Родерик МакКинон были удостоены Нобелевской премии по химии за открытие системы особых протеинов аквапоринов (AQP) — белков, регулирующих межклеточный транспорт воды в тканях.
Это открытие было сделано еще в 1988 г., а в 1993 г. П. Эгр предложил название семейству аллостерически регулируемых белков, формирующих каналы цитоплазматической мембраны, которые избирательно пропускают в цитоплазму молекулы воды, но препятствуют потоку ионов других веществ. Их назвали «аквапорины» (aquaporins) от лат. aqua — вода, греч. poros — проход, отверстие и лат. -in(e) — суффикса, обозначающего «подобный».
— Что же представляют собой такие белки?
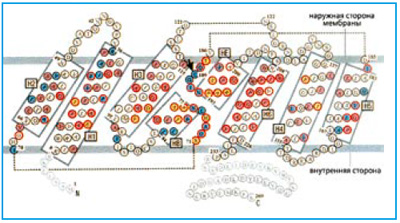
Схема расположения фрагментов, составляющих мономер аквапорина
— Первый из открытых белков, образующих трансмембранный канал для активного транспорта воды, был назван «аквапорин-1» (AQP-1). Определив структуру AQP-1 с помощью метода рентгеновской кристаллографии, П. Эгр вычислил длину и положение всех спиральных фрагментов и соединяющих их петель, а также угол, под которым соседние спирали отклоняются друг от друга; нашел места, где участки полипептидной цепи пересекают мембрану; выяснил роль консервативных в белках аквапоринового семейства аминокислотных остатков и влияние их отдельных боковых групп на стабильность и работу канала. В результате теперь мы в деталях знаем, как выглядит канал, пропускающий воду, но не ионы.
Вслед за первой молекулой были открыты другие белки семейства аквапоринов: AQP-2, AQP-3, AQP-4 и т.д. На сегодня у млекопитающих описано 13 аквапоринов, но предполагается, что это еще не все. Были найдены и клонированы гены аквапоринов. А затем началось самое интересное — выяснение их физиологической роли в организме.
Читайте также: Как исследуют ионные каналы, или Необычные «помощники» фармакологов
— Какова же эта физиологическая роль?
— Аквапорины — биохимический фундамент для нормального функционирования «метаболического котла» всех органов и тканей. Они способны проводить 3 млрд молекул воды в 1 с в расчете на каждый мономер, и присутствуют во всех без исключения живых клетках.
Прежде всего локализацию аквапорина изучили в почках, так как в функциональной единице почки — нефроне — фильтруется кровь, образуя первичную мочу, которая затем путем обратного всасывания воды концентрируется. Именно аквапорины обеспечивают реабсорбцию воды в мочевых канальцах и мочевых протоках почек. В почках работают шесть разных аквапоринов. Мутация одного из них приводит к заболеванию — несахарному диабету. У таких больных моча в почках не концентрируется, в результате чего их организм выводит очень много жидкости, организм обезвоживается, и они постоянно испытывают жажду.
Аквапорин-4 присутствует в клетках роговицы глаза и мозга, аквапорин-5 — в клетках секреторных желез, производящих слезы, пот и слюну. Аквапорин-3 содержится в клетках эпителия и защищает кожу от обезвоживания, чем весьма заинтересовались, в частности, косметологи. Этот же белок есть в эритроцитах.
П. Эгр, который в свое время возглавлял Институт изучения малярии Джонса Хопкинса, а также его коллеги большое внимание уделяли изучению роли аквапоринов в эритроцитах и в мозге при малярии, когда эритроциты лопаются, и развивается отек мозга. Аквапорины-7 и -9, относящиеся к классу глицероаквапоринов, присутствуют в клетках жировой ткани, участвуют в обмене жиров и активируются при голодании. Аквапорин-9 содержится в печени, где принимает участие в детоксикации.
Читайте также: Зачем организму ионные насосы?
Аквапорины — вездесущи, есть они у насекомых и бактерий, а также у растений, которым абсолютно необходимы, так как растения зависимы от наличия воды и не могут перемещаться в ее поисках.
— Каково значение аквапоринов для клинической медицины?
— Природа многих заболеваний связана с аквапоринами. Прежде всего это болезни почек, нарушения зрения, повреждения и отек мозга, ожирение, гипертермия, малярия, различные интоксикации. Следует учесть, что исследование аквапоринов находится на стадии интенсивного развития, поэтому перечень заболеваний, связанных с аквапоринами, может со временем существенно расшириться. Так, например, недавно исследователи из Университета Линкепинга (Швеция) определили, что клетки способны перемещаться за счет силы воды. Вообще способность клеток к перемещению и изменению формы важна для многих биологических процессов. Белые кровяные тельца, например, собираются в «горячих точках», таких как очаг воспаления или инфекции. Стволовые клетки эмбриона перемещаются в различных направлениях, чтобы сформировать органы.
Одним из нежелательных является перемещение клеток опухолей, что приводит к метастазированию рака. Клетки имеют четкие края (ведущий край и задний край) и движутся посредством широких, тонких мембранных протрузий, выбрасываемых вперед и подтягивающих клетки. Из протрузии могут также выдаваться небольшие пальцеобразные филоподии, вероятно, представляющие собой тип клеточных антенн, которые ощущают внешнее химическое воздействие (например, секрета бактерий).
Но что руководит этой способностью передвигаться? Вода — утверждают шведские исследователи во главе с Томми Карлссоном, изложившие свои гипотезы в научном журнале PLOS ONE. Оказалось, что AQP-9 повышает способность к перемещению белых кровяных клеток, скапливаясь в мембране клетки и приводя к формированию протрузий. Данные о решающей роли аквапорина в этом процессе открывают пути к новым стратегиям препятствования распространению раковых опухолей.
— Существуют ли на сегодня лекарства, для которых аквапорины служат мишенью?
— Сам первооткрыватель аквапоринов П. Эгр считает, что аквапорины — это мишени для фармакологических препаратов будущего. В этой связи я хотел бы упомянуть об одном важном направлении использования аквапоринов в клинике, связанном с лечением больных с гиперплазией и раком предстательной железы. Фирма Sophiris разработала препарат PRX302 (topsalysin), представляющий собой рекомбинантный белок, который, будучи введенным в ткань железы, способен связываться с глицерофосфатидил инозитолом и, таким образом, как бы «заякориваться» в плазматической мембране. Под действием ферментов предстательной железы, специфичных для ее ткани (простато-специфический антиген — ПСА), PRX302 формирует в мембране водные каналы. Неконтролируемый вход воды приводит к разрушению ткани железы без повреждения окружающих тканей.
Читайте также: Почему организм привыкает к лекарственным средствам и можно ли с этим бороться?
Отрадно отметить, что в этих исследованиях принимали участие и украинские ученые из Института урологии НАМНУ. Так, в частности, канд. мед. наук А.М. Ситенко поделился со мной впечатлениями о результатах инъекций препарата PRX-302 пациентам с доброкачественной гиперплазией предстательной железы в аденоматозные узлы. Наблюдение за пациентами в течение года после однократного введения препарата показало уменьшение объема аденоматозных узлов, увеличение максимальной скорости мочеиспускания, улучшение субъективных характеристик мочеиспускания и повышение качества жизни. Системных токсических эффектов препарата не обнаружено. Столь обнадеживающие результаты явились основанием для продолжения экспериментальных исследований в данном направлении. Планируется также определить эффективность препарата PRX-302 при раке предстательной железы.
Таким образом, исследования аквапоринов активно развиваются в самых различных направлениях. Это позволяет надеяться, что в ближайшем будущем могут появиться новые, более эффективные методы лечения многих заболеваний.
Подготовил Руслан Примак, канд. хим. наук
“Фармацевт Практик” #3′ 2017