Пеніциліни — антибіотики, з яких усе починалось
Минуло 90 років із відкриття Олександром Флемінгом першого антибіотика — пеніциліну. За цей час людство встигло пережити ейфорію від можливостей чудо-ліків, звикнути до того, що інфекції вже не є ворогами людства номер один, а потім, через поширення стійких до антибіотиків штамів бактерій, знов відчути безпомічність перед невидимими вбивцями. На сьогодні відомі сотні антибіотиків, але проведення ефективної антибактеріальної терапії часто є непростим завданням. Призначення антибіотиків — привілей лікаря, але фармацевти регулярно консультують пацієнтів та їхніх близьких щодо властивостей цих засобів. Отже, згадаємо особливості антибактеріальних препаратів основних груп.
Розглянемо пеніциліни — історично найстаршу, але досі одну з найбільш широко застосованих груп антибіотиків
Пеніцилінова революція
Перший антибактеріальний препарат — пеніцилін — був виділений британським бактеріологом Олександром Флемінгом із культури цвілевих грибів Penicillium notatum у 1928 р., але знадобилося близько 10 років, щоб наукова спільнота побачила потенціал у цьому відкритті. Промислове виробництво пеніциліну було налагоджено в США в 1943 р. завдяки роботі відомої Оксфордської групи, яку очолювали британський біохімік Едвард Чейн та австралійський патолог Говард Флорі. Відкриття пеніциліну стало початком нової ери в медицині та поштовхом до створення нових потужніших антибактеріальних лікарських засобів.
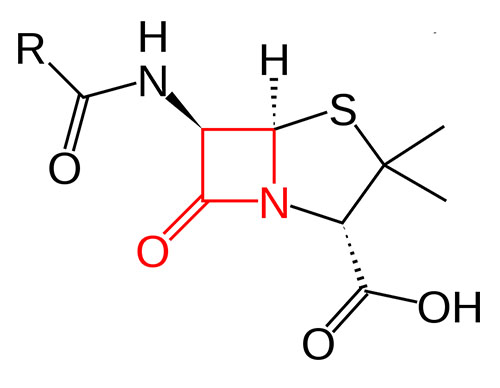
Структура пеніцилінів, β-лактамне кільце виділено червоним
Після Другої світової війни антибіотик став доступний широким масам, а в 1949 р. британський біохімік Дороті Ходжкін за допомогою методу рентгеноструктурного аналізу визначила будову молекули пеніциліну. Виявилося, що в її основі лежить 6-амінопеніциланова кислота, яка містить тіазолідиновий та β-лактамний цикли.
β-Лактамний цикл в структурі притаманний не тільки пеніцилінам, а й антибіотикам інших груп: цефалоспоринам, карбапенемам, монобактамам. До групи пеніцилінів відносяться природні сполучення, продуковані різними видами грибів Penicillium, та деякі напівсинтетичні антибіотики.
Як пеніциліни знищують бактерії
Пеніциліни чинять бактерицидну дію, блокуючи синтез пептидоглікану — основного компонента клітинної стінки бактерій. Пептидоглікан (або муреїн) — гетерополімер N-ацетилглюкозаміну та N-ацетилмурамової кислоти, які зшиті короткими пептидними ланцюжками. Велика кількість зшивок між полімерами зумовлює міцність клітинної стінки. Пептидоглікан забезпечує збереження цілості та форми бактеріальної клітини, захищає її від осмотичного лізису.
Приєднання пептидних ланцюжків до N-ацетилмурамової кислоти здійснює спеціалізований фермент транспептидаза. Пеніцилін просторово подібний до субстрату цього ферменту — D-аланіл-D-аланіну, тому утворює ковалентний ацильний зв’язок із активним центром транспептидази і таким чином необоротно інгібує її. Порушення формування пептидоглікану спричиняє поступове руйнування клітинної стінки та загибель бактерії внаслідок осмотичного лізису. Вказана транспептидаза цілком очікувано отримала назву «пеніцилін-зв’язувальний білок» (ПЗБ).
Еукаріотичні клітини (клітини, які мають ядро) не мають ані ПЗБ, ані пептидоглікану, отже, є нечутливими до пеніцилінів.
Класифікація пеніцилінів
 З природних пеніцилінів у клінічній практиці застосовують бензилпеніцилін та феноксиметилпеніцилін. Інші препарати групи — полусинтетичні сполуки, які отримують шляхом хімічної модифікації природних антибіотиків або проміжних сполук їхнього біосинтезу.
З природних пеніцилінів у клінічній практиці застосовують бензилпеніцилін та феноксиметилпеніцилін. Інші препарати групи — полусинтетичні сполуки, які отримують шляхом хімічної модифікації природних антибіотиків або проміжних сполук їхнього біосинтезу.
Природні пеніциліни (перше покоління) активні проти більшості грампозитивних бактерій, особливо коків (стафілококи, пневмококи та інші стрептококи), паличок (лістерії, клостридії, збудники дифтерії, сибірки тощо), деяких грамнегативних бактерій (гонококів, менінгококів та спірохет), актиноміцетів. Низька активність проти грамнегативних бактерій зумовлена наявністю в останніх зовнішньої мембрани, яка перешкоджає проникненню пеніцилінів всередину клітини, а також набуттям гена ферменту, який руйнує пеніциліни — бета-лактамази.
Невдовзі після початку застосування у клінічній практиці природних пеніцилінів стійки штами, що продукували бета-лактамазу, почали з’являтися й серед грампозитивних бактерій. Це спонукало до розробки полусинтетичних пеніцилінів, стійких до дії бета-лактамаз, — оксациліну, метициліну, диклоксациліну (друге покоління). Їх називали протистафілококовими пеніцилінами завдяки здатності протистояти бета-лактамазам Staphylococcus aureus.
Відносно вузький спектр активності пеніцилінів другого покоління, а також необхідність лікування інфекцій, спричинених грамнегативними збудниками, вимагали пошуку нових протимікробних засобів. Отже, у 60–70-х роках минулого століття в клінічну практику були впроваджені пеніциліни широкого спектра дії — амінопеніциліни (третє покоління). Найпопулярніші представники цього покоління — амоксицилін та ампіцилін — були ефективні проти ширшого кола грамнегативних бактерій, зокрема Haemophilus influenzae, Escherichia coli, Salmonella spp. та Shigella spp.
Пеніциліни четвертого покоління, а саме карбоксипеніциліни (карбеніцилін, тикарцилін) та уреїдопеніциліни (азлоцилін, піперацилін, мезлоцилін), активні переважно проти Pseudomonas aeruginosa, тому їх називають псевдомонадними пеніцилінами.
Окрему групу складають препарати пеніцилінів, що містять інгібітори бета-лактамаз: амоксицилін/клавуланова кислота, ампіцилін/сульбактам, піперацилін/тазобактам, тикарцилін/клавуланова кислота.
Читайте також: Бактериальные биопленки – одна из причин неэффективности антибиотиков
Стійкість бактерій до пеніцилінів
Вже у 1942 р. були виявлені штами S. aureus, нечутливі до пеніциліну. Вони швидко поширювалися лікарнями. Наприкінці 60-х років більше 80% штамів S. aureus, виділених у хворих, були стійкими до пеніциліну. Поява метициліну, здавалося, мала вирішити проблему, але стійкі до метициліну стафілококи зафіксували вже через кілька років. Механізм їхньої стійкості розкрили у 80-ті роки: виявилося, вони мають мутантний ПЗБ з низькою спорідненістю до пеніцилінів. Ген зміненого ПЗБ (mecA) розташований на мобільному генетичному елементі, тому швидко поширюється. Вже у 90-х роках у США третина госпітальних штамів S. aureus була резистентною до метициліну (такі штами називають MRSA), та до сьогодні поширеність MRSA зростає.
У 1976 р. стали надходити повідомлення про стійкі до пеніциліну штами гонококів. Їхня кількість зростала з шаленою швидкістю через поширеність гонореї та масове самолікування її пеніциліном. За короткий час сформувалися декілька механізмів стійкості гонококів до пеніциліну: окрім продукції бета-лактамази, в бактеріях з’явилися мутантні ПЗБ, а також ефлюксні насоси, які виводили пеніцилін із бактеріальної клітини.
Ще одна група бактерій з високим рівнем стійкості до пеніцилінів — ентеробактерії. Так, у 2001 р. близько двох третин інфекцій E. coli у людини вже були резистентними до ампіциліну. Натепер стійкість ентеробактерій до амінопеніцилінів продовжує поширюватися.
Небажані реакції та особливості застосування*
Пеніциліни характеризуються найнижчою токсичністю серед антибактеріальних засобів. Серед основних побічних ефектів, які вони спричиняють, слід виділити:
- алергічні реакції: кропив’янка, висип, набряк Квінке, лихоманка, еозинофілія, бронхоспазм, анафілактичний шок. Алергія є перехресною для всіх бета-лактамних антибіотиків;
- неалергічний «ампіциліновий» висип, який може зникнути без відміни препарату;
- розлади з боку травного тракту: нудота, блювання, діарея, псевдомембранозний коліт;
- порушення згортання крові та підвищення ризику кровотеч можливе при використанні карбеніциліну та, з меншою ймовірністю, уреїдопеніцилінів;
- підвищення рівня артеріального тиску та зниження ефективності антигіпертензивних препаратів можуть спричинити високі дози бензилпеніциліну натрієвої солі, карбеніциліну та інших псевдомонадних пеніцилінів;
- кандидоз порожнини рота може розвинутися внаслідок тривалого застосування пеніцилінів.
Пеніциліни виводяться переважно нирками в незміненому вигляді, тому при нирковій недостатності необхідно коригувати режим дозування.
Пеніциліни дозволені для використання в період вагітності за наявності показань до обов’язкового їх застосування.
Пеніциліни проникають у грудне молоко в низьких концентраціях. Під час лікування слід припинити годування груддю
Взаємодія з іншими лікарськими засобами*
- Пеніциліни не слід змішувати в одному шприці або в одній інфузійній системі з іншими ін’єкційними розчинами: НПВП, натрійвмісними розчинами, іншими антибіотиками тощо.
- При застосуванні бензилпеніциліну калієвої солі у високих дозах в поєднанні з калійзберігаючими діуретиками, препаратами калію або інгібіторами АПФ підвищується ризик гіперкаліємії.
- При поєднанні псевдомонадних пеніцилінів із антикоагулянтами, антиагрегантами та тромболітиками зростає ризик кровотеч.
- Холестирамін зв’язує пеніциліни в травному тракті та зменшує їхню біодоступність при пероральному прийомі.
- Пероральні пеніциліни можуть знижувати ефективність пероральних контрацептивів за рахунок порушення ентерогепатичної циркуляції естрогенів.
- Пеніциліни здатні сповільнювати виведення з організму метотрексату внаслідок пригнічення його канальцевої секреції.
- При поєднанні ампіциліну з алопуринолом підвищується ризик «ампіцилінового» висипу.
Антибактеріальні засоби групи пеніцилінів протипоказані пацієнтам із алергічною реакцією на них.
* Повний перелік протипоказань, побічних реакцій та взаємодій дивіться в інструкціях для медичного застосування відповідних лікарських засобів.
Тетяна Ткаченко, канд. біол. наук
Читайте також: Борьба с устойчивостью к противомикробным средствам: роль провизоров и фармацевтов
“Фармацевт Практик” #1′ 2019