Лінезолід і даптоміцин: «нові обличчя» серед антимікробних засобів
За останні два десятиліття кількість принципово нових антимікробних засобів, виведених на ринок, була незначною. Низка нових перспективних антибіотиків так і не дійшла до пацієнтів через те, що стійкість бактерій до них була високою ще на стадії клінічних випробувань. Криза резистентності набула таких масштабів, що довелося призначати маловживаний колістин, який в деяких випадках є єдиною надією на порятунок від мультирезистентних інфекцій. Серед препаратів, схвалених вже в ХХІ ст., розглянемо два антимікробних препарати нових класів — лінезолід і даптоміцин
Лінезолід
Лінезолід — синтетичний антибіотик, відкритий у 1990 р. та схвалений до використання в багатьох країнах світу протягом 2000–2001 рр. Тоді він був єдиним на ринку антибіотиком класу оксазолідинону, у 2014 р. до нього приєднався тедизолід (станом на листопад 2019 р. в Україні не зареєстрований). Лінезолід, як і ванкоміцин та колістин, називають антибіотиком «останнього резерву», щоб підкреслити необхідність обмеження його використання тими випадками, коли інші антибіотики неефективні, задля запобігання поширенню стійкості до нього.
 Величезна перевага лінезоліду — його майже 100% біодоступність при пероральному застосуванні. Отже, пацієнти, яким уводять лінезолід внутрішньовенно, після стабілізації стану можуть бути переведені на його пероральний прийом (таблетки лінезоліду). При цьому лінезолід можна застосовувати з перших днів життя.
Величезна перевага лінезоліду — його майже 100% біодоступність при пероральному застосуванні. Отже, пацієнти, яким уводять лінезолід внутрішньовенно, після стабілізації стану можуть бути переведені на його пероральний прийом (таблетки лінезоліду). При цьому лінезолід можна застосовувати з перших днів життя.
Окрім оригінального лінезоліду на ринку представлені його генеричні копії.
Механізм дії лінезоліду. Лінезолід є інгібітором синтезу білка в бактеріях, завдяки чому припиняє їхній ріст та розмноження. Лінезолід інгібує трансляцію на етапі ініціації, що відрізняє його, наприклад, від макролідів, які діють на етапі елонгації. Лінезолід перешкоджає утворенню ініціаторного комплексу, що складається з двох субодиниць рибосоми (30S і 50S), транспортної РНК та матричної РНК, з якої зчитується інформація про послідовність амінокислот в ланцюгу. Як показав рентгеноструктурний аналіз, лінезолід зв’язується з А-сайтом на 50S-субодиниці рибосоми, що спричиняє просторові зміни, які заважають приєднанню до А-сайту ацильованої тРНК.
Спектр активності лінезоліду. Препарат призначають для лікування важких інфекційних захворювань, спричинених грампозитивними бактеріями, стійкими до інших антибіотиків. Лінезолід є активним щодо більшості клінічно значущих грампозитивних бактерій, зокрема стрептококів, стійких до ванкоміцину ентерококів, метицилінорезистентного Staphylococcus aureus (MRSA), лістерій та коринебактерій. Лінезолід не чинить клінічно значущої дії на більшість грамнегативних бактерій.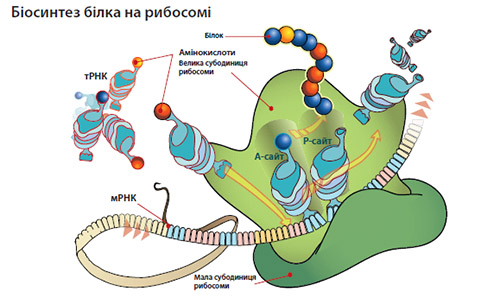
Показаннями для застосування лінезоліду є лікування інфекцій, спричинених чутливими штамами грампозитивних мікроорганізмів, включаючи інфекції, що супроводжуються бактеріємією: пневмонія (зокрема нозокоміальна), інфекції шкіри та її структур, інфекції, спричинені ентерококами.
Стійкість до лінезоліду. Перші повідомлення про випадки інфекцій, стійких до лінезоліду, з’явилися майже одразу після його впровадження в клінічну практику (у Enterococcus faecium та S. aureus). Проте стійкість до лінезоліду залишається стабільною та надзвичайно низькою (менше 1%).
Резистентність грампозитивних бактерій до лінезоліду може розвиватися внаслідок точкової мутації в гені, що кодує 23S-рибосомальну РНК. Такий механізм притаманний стафілококам та E. faecium. Також стійкість може бути пов’язана з мутаціями в генах, що кодують рибосомальні білки L3 та L4. Обидва варіанти стійкості порушують взаємодію антибіотика з мішенню — 50S-субодиницею рибосоми.
Бактерії можуть отримати стійкість до лінезоліду від інших бактерій шляхом горизонтального переносу гена cfr. Останній вже давно відомий, а його назва означає, що він призводить до розвитку стійкості до хлорамфеніколу і флорфеніколу. Цей ген кодує фермент, який метилює рибосомальну РНК бактерії таким чином, що вона не втрачає здатності забезпечувати синтез білка, але стає невразлива до низки антибіотиків, зокрема лінезоліду. Також шляхом горизонтального переносу бактерії (описано для Enterococcus faecalis і E. faecium) можуть отримати плазмідний ген optrA, що кодує транспортну систему АВС, здатну виводити з мікробної клітини лінезолід.
Природна стійкість більшості грамнегативних бактерій до лінезоліду пояснюється активністю ферментів-насосів, які виводять препарат з клітини швидше, ніж він накопичується.
Протипоказанням* до застосування є гіперчутливість до лінезоліду.
Побічні ефекти та особливості застосування лінезоліду*. При короткотривалому використанні лінезолід є відносно безпечним. Можливими небажаними ефектами є діарея, нудота, блювання, запор, головний біль, висипка, зміна сприйняття смаку. Підвищується ризик розвитку кандидозу. При застосуванні лінезоліду довше 14 діб можлива тромбоцитопенія, протягом кількох місяців — периферична та оптична невропатії, подекуди незворотні.
Даних щодо безпеки використання лінезоліду у вагітних недостатньо. Дослідження на тваринах показали помірну токсичність для плода, але застосування препарату можливе, якщо очікувана користь для вагітної перевищує потенційний ризик для плода. В період застосування препарату необхідно припинити годування груддю.
Взаємодії*. Препарат не слід призначати пацієнтам, які приймають або приймали будь-які медичні засоби, що пригнічують моноаміноксидазу А та В. Лінезолід не впливає на метаболізм лікарських засобів, опосередкований системою цитохрому P450.
Даптоміцин
Даптоміцин є першим препаратом антимікробних засобів нового класу — ліпопептидів. Його було виділено із актинобактерій Streptomyces roseosporus в рамках програми скринінгу мікроорганізмів ґрунту. Випробування препарату розпочалися в 1985 р., але були зупинені в І фазі після виявлення у добровольців випадків міопатії. Пізніше, коли стійкість до ванкоміцину стала зростати, необхідність в розробці нових лікарських засобів, активних щодо MRSA, призвела до перегляду клінічної цінності даптоміцину, і випробування відновилися з використанням препарату в зниженій дозі. В 2003 р. даптоміцин було схвалено в США, потім — і в інших країнах. Наразі доступний лише оригінальний даптоміцин, через що лікування ним є вельми дороговартісним.
 Даптоміцин вводять парентерально шляхом повільної в/в інфузії один раз на добу.
Даптоміцин вводять парентерально шляхом повільної в/в інфузії один раз на добу.
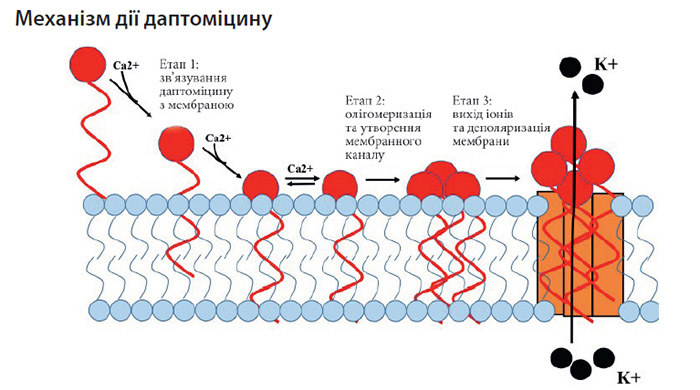
Механізм дії даптоміцину є унікальним. Він є циклічним ліпопептидом, що складається з 13 амінокислотних залишків, має гідрофільне ядро і гідрофобний хвіст. Останній за допомогою кальційзалежного механізму необоротно зв’язується з клітинною мембраною грампозитивних бактерій, в результаті чого формується канал, через який із цитоплазми швидко виходять іони калію та інші іони. Це призводить до втрати мембранного потенціалу і відповідно до пригнічення синтезу білка, руйнування ДНК і РНК та швидкої загибелі бактерії (при цьому не спостерігається осмотичного лізису, як, наприклад, у разі дії бета-лактамних антибіотиків).
Відсутність у даптоміцину ефекту щодо грамнегативних бактерій пов’язана з наявністю у них зовнішньої мембрани, через яку молекула антибіотика не може проникнути.
Спектр активності даптоміцину. Антибіотик проявляє бактерицидну дію щодо S. aureus (зокрема MRSA), S. haemolyticus, коагулазонегативних стафілококів, Streptococcus agalactiae, Streptococcus pyogenes, стрептококів групи G, Clostridium perfringens, Peptostreptococcus spp.
Даптоміцин призначають при ускладнених інфекціях шкіри та підшкірних тканин; правосторонньому інфекційному ендокардиті, зумовленому S. aureus у дорослих; бактеріємії, спричиненій S. aureus. Не призначають при пневмонії через зниження його активності в присутності сурфактанта.
Стійкість бактерій до даптоміцину залишається низькою. Перший випадок стійкості був зафіксований у 2005 р. в Кореї. З того часу повідомлення носять поодинокий характер. Цікаво, що стійкість до даптоміцину була притаманна бактеріям роду Paenibacillus, знайденим в печері Лечугілья в США, яка була ізольована від світу останні 4 млн років. Механізми стійкості бактерій до даптоміцину ще не визначені.
Протипоказанням* до застосування є гіперчутливість до даптоміцину.
Побічні ефекти та особливості застосування даптоміцину*. Препарат характеризується доброю переносимістю. Найчастішими небажаними реакціями є грибкові інфекції, інфекції сечовивідного тракту, анемія, тривожність, безсоння, запаморочення, головний біль, артеріальна гіпертензія або гіпотензія, біль в животі, нудота, блювання, запор, діарея, метеоризм, відхилення результатів печінкових проб від норми (підвищення рівня АЛТ, АСТ або лужної фосфатази), висипка, біль у кінцівках, підвищений рівень креатинфосфокінази у сироватці крові, реакції в місці введення, гарячка, астенія. Рідко можливий розвиток більш серйозних ефектів: реакції гіперчутливості, еозинофільної пневмонії, ангіоневротичного набряку та рабдоміолізу.
Клінічних даних щодо впливу даптоміцину на перебіг вагітності немає, дослідження на тваринах не вказують на його прямий або непрямий шкідливий вплив. Але препарат призначають, лише якщо очікувана користь для вагітної перевищує потенційний ризик для плода. В період застосування препарату потрібно припинити годування груддю.
Даптоміцин не використовують у дітей віком до 1 року.
Взаємодії*. Даптоміцин не впливає на метаболізм лікарських засобів, опосередкований системою цитохрому P450. При застосуванні даптоміцину рекомендовано тимчасово призупинити застосування лікарських засобів, здатних спричинити міопатію, за неможливості перевіряти рівень КФК частіше ніж один раз на тиждень.
Даптоміцин несумісний з розчинниками, що містять глюкозу.
Підготувала Тетяна Ткаченко, канд. біол. наукa
* Повний перелік протипоказань, побічних реакцій та взаємодій див. в інструкціях для медичного застосування відповідних лікарських засобів.
“Фармацевт Практик” #11′ 2019