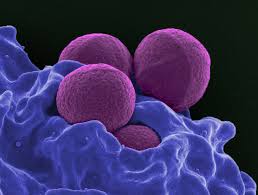
Чем опасен золотистый стафилококк?
Микроб — ничто, субстрат (то есть организм) — все
Луи Пастер
Золотистый стафилококк принадлежит к довольно многочисленному роду Stafilococcus, который объединяет около 30 видов грамположительных бактерий шаровидной формы, образующих скопления, напоминающие грозди винограда (греч. staphelos — гроздь). Добрая половина из них — симбионты (паразиты) человека. Однако только о золотистом стафилококке принято говорить как о «патогенном стафилококке». Именно с ним связаны многие медицинские проблемы
Золотистый стафилококк (Stafilococcus аureus) — одна из самых распространенных бактерий — нередко выделяется и у здоровых людей. Избежать контакта с ним мало кому удается, особенно в медицинских стационарах. Другое дело, что примерно 20% людей избавляются от стафилококка практически сразу, большинство (около 60%) — через несколько дней или недель, и только 20% становятся носителями S. аureus на месяцы, а иногда и годы.
Носители, особенно выделяющие массивные дозы бактерий, представляют наибольшую опасность для окружающих. Прежде всего для тех, кто не способен «противостоять» инфекции. По числу факторов с потенциальной болезнетворностью золотистому стафилококку нет равных.
Практически неограниченными возможностями в колонизации тканей хозяина S. аureus обязан поверхностным белкам-адгезнам, ответственным за его прикрепление к различным биологическим субстратам.
Также читайте: Носительство золотистого стафилококка: опасный источник
Благодаря собственным липазам он может разрушить сальную пробку в устье волосяного мешочка и обеспечить себя «продуктами питания». Устойчивость к жирным кислотам и высоким концентрациям хлорида натрия помогает ему выжить в секретах потовых и сальных желез. Гиалуронидаза расширяет зону инфекции за счет разрушения соединительной ткани. Стафилокиназа разрушает фибриновые сгустки с образованием инфицированных микротромбов. Капсула служит надежной механической защитой от фагоцитов. Правда, генетически закрепленная способность к капсулообразованию реализуется немногими штаммами и считать ее универсальным фактором патогенности вряд ли можно. Зато индуцировать (с помощью коагулазы) образование сгустков фибрина, препятствующих контакту с фагоцитами, способны практически все штаммы золотистого стафилококка. То же самое можно сказать о лейкоцидине — токсине «избирательного действия» (специализируется на лизисе нейтрофилов и макрофагов) и стафилолизинах, известных еще как гемолизины.
Золотистый стафилококк (S. аureus) — одна из самых распространенных бактерий — нередко выделяется и у здоровых людей. Избежать с ним контакта мало кому удается, особенно в медицинских стационарах
S. аureus продуцирует четыре разновидности гемолизинов (альфа, бета, гамма и дельта), которые отличаются по степени токсичности, антигенным и физико-химическим свойствам. Наиболее важен патогенетически альфа-гемолизин. Судя по результатам модельных экспериментов, он повреждает лейкоциты, эритроциты, тромбоциты, тучные клетки, фибробласты, гепатоциты, эндотелиоциты; при подкожном введении вызывает некроз, при внутривенном — оказывает токсическое действие на центральную нервную систему, миокард, сосуды, надпочечники и т.д. Однако в клинической практике отнюдь не всегда прослеживается связь между развитием стафилококковой инфекции и динамикой накопления антител к альфа-гемолизину. Впрочем, в равной степени это справедливо и в отношении остальных стафилококковых антигенов.
Золотистый стафилококк: последствия вторжения
Чаще всего S. аureus «поселяется» на слизистой оболочке носа и носоглотки, реже — на коже. Однако слизистые оболочки поражаются редко. При ангине, отите, бронхите и пневмонии золотистый стафилококк обычно играет вспомогательную роль, осложняя течение основного патологического процесса, тогда как самой распространенной формой стафилококковой инфекции является пиодермия, в зависимости от локализации и характера поражения подразделяемая на:
– импетиго (поверхностное поражение кожи типа гнойничковой сыпи; волосяных фолликулов лица, подмышечных впадин или лобка);
– фурункул (гнойное воспаление волосяного фолликула и окружающих его тканей);
– фолликулит (гнойное воспаление волосяного фолликула);
– сикоз (гнойное воспаление);
– ячмень (гнойное воспаление сальной железы волосяного фолликула ресницы);
– карбункул (слияние нескольких фурункулов);
– гидраденит (гнойное воспаление апокринных потовых желез, которые открываются в волосяные фолликулы);
– пузырчатку новорожденных (гнойничковая сыпь, локализующаяся, как правило, в паховых складках, подмышечных впадинах, на коже живота и шеи).
При сахарном диабете, возрастной эволюции апокринных потовых желез, гиперфункции сальных желез и изменении качества их секрета (в период полового созревания) риск развития пиодермии возрастает. Высокие инфицирующие дозы, внедрение инородных тел и микротравмы кожи тоже увеличивают вероятность местных инвазий. Хотя в отличие от других бактерий S. аureus может поражать и неповрежденную кожу, проникая через устья волосяных фолликулов или протоки потовых желез.
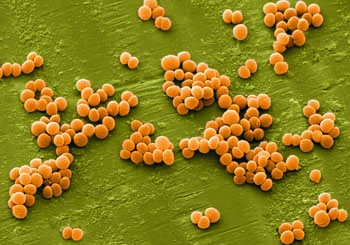 Иногда пиодермия осложняется бактериемией (заражением крови). Как следствие — возникают новые очаги гнойного воспаления.
Иногда пиодермия осложняется бактериемией (заражением крови). Как следствие — возникают новые очаги гнойного воспаления.
Очень часто первым, а порой и единственным признаком бактериемии является остеомиелит, по образному выражению Л. Пастера «фурункул костного мозга». Без адекватной антибактериальной терапии «фурункул» может превратиться в постоянный источник инфекции и усугубить течение бактериемии. Массивная бактериемия, в свою очередь, может вызвать поражение клапанов сердца, чаще — органически измененных (вследствие ревматизма или хирургического вмешательства), реже — нормальных.
Еще один возможный сценарий развития событий связан с так называемым опасным треугольником — областью с основанием вдоль верхней губы и вершиной над переносицей, — точнее, с пиогенным процессом, локализованным в этой зоне.
«Опасный треугольник» характеризуется слабым развитием соединительной ткани, отсутствием клапанов на венах, напрямую связанных с мозговыми синусами и постоянным движением мимических мышц. Все это ослабляет механические барьеры на пути стафилококковой инфекции, создавая угрозу смертельных поражений головного мозга (энцефалит) и его мягких оболочек (менингит).
Наряду с пиогенными инфекциями золотистый стафилокок способен вызывать специфические интоксикации: синдром «ошпаренной кожи», пищевое отравление, синдром токсического шока.
Синдром «ошпаренной кожи» поражает детей первого года жизни, преимущественно новорожденных. Клиническая картина и патогенез заболевания связаны с токсином под названием «эксфолиатин». К счастью, его продуцируют лишь 5% штамммов S. аureus, вследствие чего синдром «ошпаренной кожи» встречается довольно редко. Эксфолиатин разрушает межклеточные контакты зернистого эпителия не только в очаге инфекции, но и за его пределами, что приводит к отслоению эпидермиса и образованию изъязвлений на значительной поверхности туловища и конечностей. Десквамация продолжается несколько дней. Через две недели пораженные участки заживают без образования рубцов.
Пищевое отравление — едва ли не самая распространенная интоксикация бактериальной природы. Непосредственная причина отравления — энтеротоксин. Попадая в пищеварительный тракт с продуктами питания, энтеротоксин вызывает гастроэнтерит с тяжелой рвотой и диареей.
Энтеротоксин обладает высокой термостабильностью (в частности, выдерживает кипячение) и устойчив к действию протеолитических ферментов пищеварительного тракта.
Через несколько лет после внедрения в клиническую практику пенициллина появились первые сообщения о пенициллин-резистентных штаммах S. aureus. Сегодня практически все штаммы стафилококка вырабатывают ферменты бета-лактамазы, разрушающие природные пенициллины
Синдром токсического шока характеризуется скарлатинозноподобной сыпью, внезапным повышением температуры тела, рвотой, диареей, мышечной болью и быстро прогрессирующей артериальной гипотензией. У многих больных развиваются почечная и респираторная недостаточность, в большинстве органов наблюдаются изменения. Нередко заболевание завершается летальным исходом.
Первая вспышка такого заболевания была зарегистрирована в 1980 году в США. Все пострадавшие (болезнь поражала молодых женщин, главным образом в период менструации) пользовались высокоадсорбционными вагинальными тампонами, которые менялись реже обычных, что создавало благоприятные условия для размножения золотистого стафилококка. Позднее выяснилось, что заболевание встречается при любой локализации стафилококковой инфекции и обусловлено чрезвычайно сильным токсином, продуцировать который способны лишь немногие штаммы S. аureus.
Золотистый стафилококк: выживает сильнейший
Золотистый стафилококк славится своей способностью быстро адаптироваться к антибактериальным препаратам.
Через несколько лет после внедрения в клиническую практику пенициллина появились первые сообщения о пенициллин-резистентных штаммах S. aureus. Сегодня практически все штаммы стафилококка вырабатывают ферменты бета-лактамазы, разрушающие природные пенициллины.
С полусинтетическими пенициллинами — метициллином и оксациллином — история повторилась. Наделенные способностью подавлять разрушительное действие бета-лактамаз, они, как и ожидалось, стали эффективным средством лечения инфекций, вызванных пенициллинрезистентными штаммами стафилококка. Но не прошло и пяти лет, как были зарегистрированы штаммы S. аureus, устойчивые не только к новым препаратам, но и ко всем бета-лактамным антибиотикам: так называемые MRSA (methicillin-resistant Staphylococcus aureus). На этот раз бактерии избрали другой способ защиты — «научились» синтезировать дополнительный фермент, участвующий в синтезе главного компонента бактериальной стенки — пептидогликана — и характеризующийся пониженной способностью к связыванию с бета-лактамами. В присутствии бета-лактамных препаратов его активность остается неизменной, синтез пептидогликанов продолжается и, как следствие, сохраняется жизнеспособность MRSA.
Также читайте: Борьба с устойчивостью к противомикробным средствам: роль провизоров и фармацевтов
Нередко устойчивость к бета-лактамам ассоциируется с устойчивостью к антибиотикам других групп. По некоторым данным, частота ассоциированной резистентности среди MRSA к макролидам, линкозамидам, тетрациклинам, хлорамфениколу и гентамицину (являющемуся маркером устойчивости ко всем аминогликозидам) превышает 40–80%.
Средний уровень устойчивости к рифампицину относительно невысок — 14%. Однако резистентность к препарату может формироваться даже в процессе лечения.
С внедрением в медицинскую практику фторхинолонов появилась надежда на эффективную эрадикацию MRSA. Но по прошествии четырех лет выяснилось, что в зависимости от интенсивности применения этих препаратов частота резистентности к ним варьирует от 9 до 80%.
Устойчивость к триметоприм/сульфаметоксазолу формируется крайне редко. Тем не менее использовать его для лечения инфекций, вызванных MRSA, нецелесообразно из-за возможных побочных реакций в виде синдрома Стивенса — Джонсона или синдрома Лайелла.
А вот природный трициклический гликопептидный антибиотик ванкомицин, созданный еще в 50-х годах прошлого века, в период катастрофического роста резистентности S. аureus к пенициллину, сегодня считается препаратом выбора для эрадикации MRSA.
Также читайте: Staphylococcus aureus: золотистая смерть или не стоит беспокоиться?
Любопытно, что добрых два десятка лет ванкомицин использовали в основном для лечения стафилококковых инфекций у больных с тяжелыми аллергическими реакциями на пенициллин. И только в начале 80-х, когда резко увеличилась устойчивость S. аureus к метициллину (а заодно и ко всем бета-лактамам и антибиотикам других классов), он «приобрел» новый статус. Как долго ванкомицин будет оставаться препаратом выбора, прогнозировать никто не берется. Хотя бы потому, что лет десять назад штаммы стафилококка со сниженной чувствительностью к препарату были выделены во Франции и в Японии, несколько позже — в Южной Корее, США, Шотландии, Бразилии и ЮАР. Не так давно в США были выделены ванкомицинрезистентные штаммы S. аureus. Их пока только десять.
Ламара Львова, канд. биол. наук
“Фармацевт Практик” #02′ 2010