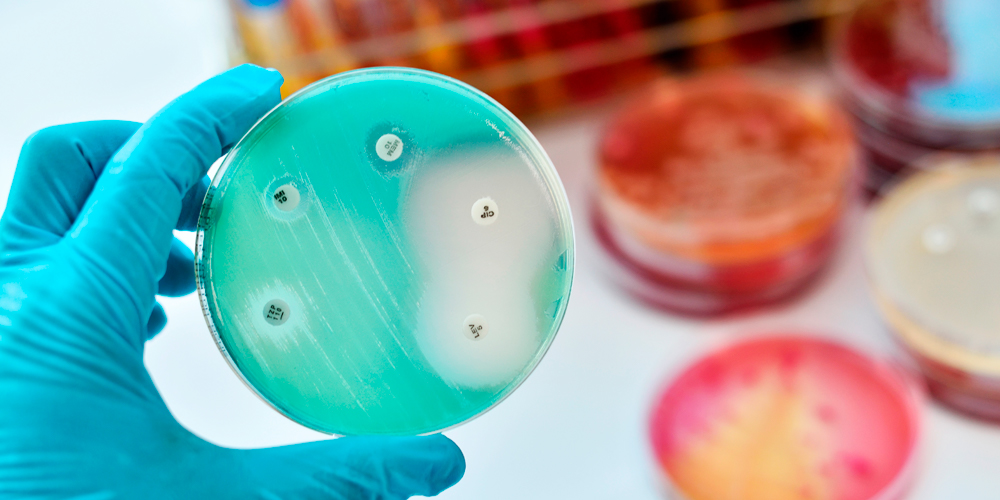
Чи вдасться подолати резистентність бактерій?
Однією з найважливіших проблем сучасної медицини є явище резистентності бактерій до антибіотиків. Нових антибіотиків стає все менше, адже жодна фармацевтична компанія не буде робити свій бізнес на препараті, який невдовзі через розвиток до нього стійкості може втратити попит на ринку. Останніми роками учені все активніше проводять пошук нових можливостей боротьби з цим явищем
Що таке «ад’ювантний» підхід?
Замість модифікувати старі антибіотики або перевіряти базу синтетичних речовин щодо антибіотичної активності учені пропонують боротися з резистентністю, що виникає у бактерій, за допомогою методу, який заснований на блокуванні механізмів стійкості. Такий підхід має назву «ад’ювантний», а сам процес — «потенціація» через здатність посилювати дію вже існуючих препаратів. Зрозуміло, що потенціатор необхідно застосовувати разом з антибіотиком, до якого у більшості бактерій вже сформувалася резистентність.
Усі механізми резистентності «включаються» у відповідь на наявність антибіотика в середовищі, тому боротися з нею можна шляхом збою настройки й порушення роботи сигнальної системи. Якщо бактерія не відчує присутності антибіотика, вона просто не буде активувати системи захисту від нього. В одержанні й обробці сигналів бактерії використовують двокомпонентні системи, що складаються з мембранного білка-кінази (зазвичай це гістидинкіназа) й внутрішньоклітинного білка-регулятора. Ці системи слугують бактеріям для одержання інформації про своє оточення. Цікаво зазначити, що за нестачі такої інформації бактеріальна клітина гине. Таким шляхом, наприклад, у результаті спільної дії валрицину А й валрицину В був переможений стійкий до метициліну Staphylococcus aureus [1]. А от потенціаторів, які б блокували передачу сигналу про наявність антибіотика в середовищі, поки що не синтезовано. Однак зауважимо, що це дуже перспективний напрям, оскільки у такий спосіб можна «повернути до життя» практично будь-який антибіотик.
«Радикальне» рішення
У деяких бактерій резистентність проявляється вже на першому етапі дії антибіотика: вони просто не дають проникнути препарату всередину клітини і здійснюють це за рахунок зменшення кількості пор у мембрані або навіть зміни будови цих пор. Саме так виникла, наприклад, резистентність у кишкової палички до цефалоспоринів — через структурні зміни спеціальних білків-поринів. Останні необхідні клітині для пропускання невеликих молекул (перш за все води), оскільки найчастіше антибіотики проникають всередину бактерій саме цим шляхом. Однак внаслідок мутацій порини кишкової палички перестали пропускати маленькі гідрофільні молекули (такі як цефалоспорини) [2].
Для подолання резистентності такого виду дослідники прийняли «радикальне» рішення: зробити отвір у мембрані бактерій за допомогою винайдених спеціальних речовин, що порушують цілість зовнішньої мембрани, завдяки чому антибіотики можуть пройти крізь неї навіть за відсутності поринів та інших білків-переносників [3].
До речі, саме у такий спосіб антибіотики стають універсальними. Головна відмінність грамнегативних бактерій від грампозитивних полягає в наявності другої мембрани, через що антибіотикам важче проникати в клітину грамнегативних бактерій. Але у разі використання потенціаторів, що порушують цілість зовнішньої мембрани, цієї проблеми не виникає.
«Біг навипередки»
Після того як антибіотик проник всередину клітини, йому необхідно виконати головне завдання — знайти й зв’язатися зі своєю мішенню, для чого потрібен певний час. Найпопулярніший, неспецифічний та простий спосіб завадити цьому з боку бактерії — викачати антибіотик, поки він не встиг знайти свою мішень. Відповідно для боротьби з таким типом резистентності необхідно якимось чином порушити роботу тих насосів, які це здійснюють. Існує кілька рішень даної проблеми. Наприклад, за допомогою РНК-інтерференції можна перешкодити експресії генів, що кодують насоси; модифікувати антибіотик таким чином, щоб бактеріальна клітина не змогла його розпізнати; завадити синтезу подібних насосів; не допустити надходження енергії до насосів. Усі ці ідеї заслуговують на увагу, але мають одну ваду: ті сполуки, за допомогою яких буде порушуватися робота насосів, також почнуть виводити з клітини ті самі насоси. Отже, буде спостерігатися «біг навипередки», тобто що відбудеться раніше – антибіотик встигне знайти свою мішень чи насоси виведуть його з клітини.
Можна також використати сполуки, що конкурують з антибіотиками за насоси [4]. У цьому випадку антибіотик все одно буде виводитися з клітини, але у менших кількостях.
Хімічна «атака» на антибіотик
Ще один шлях розвитку резистентності полягає в тому, що деякі бактерії руйнують хімічні зв’язки в антибіотику, внаслідок чого він не здатний зв’язатися зі своєю мішенню. Найвідоміший приклад подібної реакції – бета-лактамазна. Спеціальний фермент бета-лактамаза «розрізає» у бета-лактамних антибіотиків (наприклад, пеніциліну) їхнє бета-лактамне кільце. До речі, цю стійкість було відкрито ще до масового використання пеніциліну. Інший приклад подібного ферменту – естераза, яка руйнує ефірні зв’язки в макролідах. Судячи з усього, її ген перебуває у мобільному генетичному елементі [5], тому варто чекати, що, певно, скоро відбудеться поширення цього ферменту.
Інші ж бактерії здійснють боротьбу з антибіотиками протилежним шляхом – не руйнують в них зв’язки, а приєднують різноманітні групи: ацильні, фосфатні, нуклеотидні, рибозні, тіольні тощо. Для цього у бактерій існує велика кількість спеціальних ферментів – трансфераз, але діяти вони можуть тільки всередині клітини, оскільки потребують участі АТФ.
Тривалий час дослідники намагалися перемогти в цій гонитві шляхом створення сполучень, які не можуть розрізати бета-лактамази, естерази або епоксидази, а різні трансферази – модифікувати. Нині спостерігається новий виток цієї боротьби, оскільки було відкрито інгібітори бета-лактамаз, й фармацевтичні компанії розпочали пошук речовин, здатних інгібувати роботу подібних ферментів.
Бактерії «маскують» мішені антибіотиків
Є випадки, коли антибіотик проник до клітини й перебував у ній достатньо часу, але все одно не зміг знайти свою мішень. Справа в тому, що бактерії можуть модифікувати цю мішень, щоб препарат не впізнав її і не зв’язався з нею. Вони навіть «включають» спеціальні обхідні шляхи метаболізму, до яких мішень не входить. Звичайно, такі випадки є досить рідкісними, адже однією спонтанною мутацією тут не обійтися. Однак якщо це все-таки сталося, подолати подібну резистентність за допомогою потенціаторів складніше.
Цікавим прикладом такого випадку може слугувати виникнення резистентності до ванкоміцину у грампозитивних бактерій. Цей антибіотик інгібує синтез клітинної стінки за рахунок утворення водневих зв’язків з ацил-D-аланіл-D-аланіном на кінці зростаючого пептидоглікану. Через те, що його мішенню є не білок, до ванкоміцину тривалий час (понад 30 років) стійкість не вироблялася. Небагато з антибіотиків можуть «похизуватися» таким довгим життям. Навіть у наші часи ванкоміцин все ще вважають антибіотиком «останньої надії» й застосовують лише в тому випадку, коли інші препарати не допомогли.
Також бактерії можуть змінювати мішень вже після її синтезу – за допомогою спеціальних ферментів. Наприклад, у цьому полягає стійкість стафілококів до макролідів, лінкозамідів та стрептограмінів. Ці антибіотики є вельми різними за структурою, але чинять подібну дію: прикріплюються до рибосоми й «зачиняють» вихід пептидів з її великої субодиниці, внаслідок чого порушується синтез білка в клітині. Стафілококи ж «винайшли» фермент метилтрансферазу, котра приєднує до великої субодиниці рибосоми метильну групу, через що зазначені вище антибіотики зв’язатися з рибосомою не мають можливості.
На жаль, у цьому випадку винайти потенціатор також вельми складно. Можливо, ним може стати інгібітор метилтрансфераз або інгібітор роботи сигнальної двокомпонентної системи. Допоки будь-яких сполучень з подібними властивостями не виявлено.
***
Отже, дослідження механізмів виникнення резистентності у бактерій тривають. У деяких випадках одержано обнадійливі результати щодо можливостей її подолання, тому стверджувати, що ера антибіотиків вже скінчилася, певно, зарано.
Підготував Руслан Примак, канд. хім. наук
Література
- Gotoh Y., Doi A., Furuta E. et al. Novel antibacterial compounds specifically targeting the essential WalR response regulator// J. ‒ 2010. ‒ Vol. 63. ‒ P. 127-134.
- Martinez-Martinez L., Conejo M.C., Pascual A. et al. Activities of Imipenem and Cephalosporins against Clonally Related Strains of Escherichia coli Hyperproducing Chromosomal beta -Lactamase and Showing Altered Porin Profiles// Antimicrobial Agents and Chemotherapy. – 2000. – Vol. 44. – P. 2534-2536.
- Zabawa T.P., Pucci M.J., Parr T.R., Lister T. Treatment of Gram-negative bacterial infections by potentiation of antibiotics //Current Opinion in Microbiology. – 2016. – Vol. 33. – P. 7-12.
- Mahamoud A., Chevalier J., Alibert-Franco S. et al. Antibiotic efflux pumps in Gram-negative bacteria: the inhibitor response strategy // Journal of Antimicrobial Chemotherapy. – 2007. – Vol. 59. – P. 1223-1229.
- Biskri L., Mazel D. Erythromycin Esterase Gene ere (A) Is Located in a Functional Gene Cassette in an Unusual Class 2 Integron // Antimicrobial Agents and Chemotherapy. – 2003. – Vol. 47. – P. 3326-3331.