Системы групп крови: «АВ0» и «резус»
Открытие групп крови по праву считается одним из важнейших событий в истории медицины, поскольку оно способствовало снижению смертности при переливании крови. Впоследствии был открыт ряд систем антигенов, наиболее важными из которых являются «АВ0» и «резус»
Опасные эксперименты
На протяжении столетий вопрос о том, можно ли переливать больному кровь другого человека, вызывал у эскулапов неподдельный интерес. При этом некоторые считали, что с помощью переливания можно вылечить все болезни, включая психические заболевания. После ряда трагически завершившихся для пациентов трансфузий крови животных врачи не решались экспериментировать вплоть до XIX в. Исключением стал английский врач Дж. Бланделл, который был убежден в том, что главной ошибкой при переливании крови в прошлом было использование крови животных, то есть другого вида. Бланделл перелил своему пациенту 0,4 л крови, полученной от доноров. Больной, сперва почувствовавший себя намного лучше, скончался черед два дня. Но это не остановило ученого — в последующие годы он сделал еще 10 переливаний крови, однако, только четверо из его пациентов выжили.
Другие врачи также экспериментировали с переливанием крови (кое-кто даже попытался добавлять в кровь молоко), но результаты в целом были не слишком утешительными.
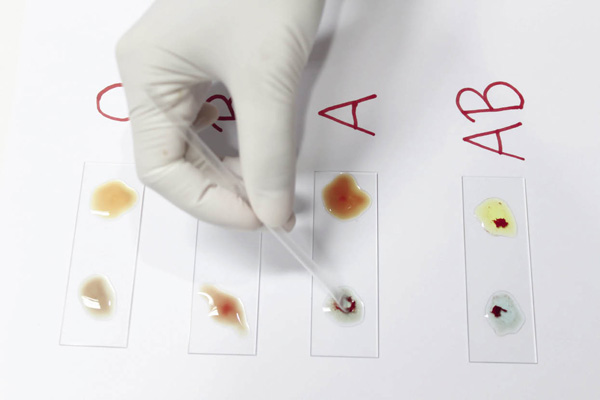
Система «АВ0»
Когда в конце XIX в. ученые попытались смешать в пробирке кровь разных людей, они заметили, что иногда в ней возникали сгустки. Впервые об этом задумался австрийский врач-иммунолог Карл Ландштайнер, который начал исследовать закономерности возникновения сгустков, смешивая кровь здоровых людей, в том числе и свою.
В 1900 г. он увидел, что сгущение происходило только при смешивании крови определенных людей, и экспериментальным путем обнаружил три основные группы, которые назвал A, B и C. Впоследствии группу C переименовали в 0, а несколькими годами позже ученые обнаружили группу AB.
Читайте также: Истоки мифов о вампирах
В нашей стране (как и на всей территории бывшего СССР) применяли систему нумерации I–IV, предложенную чешским ученым Яном Янским, который открыл систему «АВ0» параллельно с К. Ландштайнером. Соответственно в системе «АВ0» выделяют 4 группы крови: І, или 0, ІІ, или А, ІІІ, или В, IV, или АВ. Теоретически лица с I группой крови являются универсальными донорами — ее можно переливать всем, а IV — универсальным акцептором, так как ее обладателям можно переливать кровь любой группы. В современной практике человеку переливают кровь той же группы, что и его собственная.
Эволюция и «бомбейский феномен»
В настоящее время известно, что «группа крови» представляет собой совокупность антигенных характеристик эритроцитов, то есть специфических групп белков и углеводов, которые содержатся в их мембранах. Попадая в кровь других организмов, они могут вызывать различные иммунные реакции.
Антигены эритроцитов крови кодирует ген АВ0. Сравнив этот ген у людей и представителей других видов живых существ, ученые сделали вывод о том, что деление на разные группы крови возникло очень давно. Гиббоны и люди имеют варианты ІІ и ІІІ групп крови, которые происходят от общего предка, жившего 20 млн лет назад.
Возможно, наши группы крови возникли еще раньше, но выяснить точное время достаточно сложно, так как для этого нужно проанализировать гены всех видов приматов.
Однако имеющиеся данные свидетельствуют о том, что эволюция групп крови была весьма бурной, причем вследствие мутаций некоторые из них исчезли у обезьян.
Читайте также: “Кровь – самое опасное из используемых в медицине веществ”
Так, шимпанзе имеют только І и ІІ группы крови, а гориллы, напротив, лишь ІІІ.
В 1952 г. в индийском городе Бомбее (современный Мумбаи) врачи обнаружили пациентов, которые вообще не имели никакой группы крови, то есть на поверхности их эритроцитов не было антигенов системы «АВ0». Генетики связывают этот факт с близкородственными браками между членами одной касты. В принципе, такая кровь не несет никаких рисков для своего владельца, кроме единственной ситуации: если человек с бомбейским фенотипом будет нуждаться в переливании крови, то ему подойдет только кровь такого же типа. Даже І группа крови, которая считается совместимой со всеми остальными, будет для такого пациента смертельно опасной.
Следует отметить, что система «АВ0» является далеко не единственной у человека. В настоящее время описано около 346 антигенов, 306 из которых сгруппированы в пределах 36 различных систем крови, однако, они не оказывают значительного влияния при трансфузии [1]. Исключение составляет система «резус».
Резус-фактор: не только у макак
К. Ландшейнеру принадлежит еще одно важное открытие. В 1940 г. совместно с А. Винером он обнаружил антиген D, приводящий к неблагоприятным реакциям переливания крови у макак-резус. Впоследствии этот антиген был обнаружен также у человека [2].
Система «резус» (RhD) является клинически наиболее важной, а также самой сложной и полиморфной системой групп крови у людей более чем с 460 аллелями (различными формами), известными для RhD-гена [3, 4]. Она включает около 50 антигенов, среди которых чаще всего встречаются D (85%), С (70%), Е (30%), е (80%). При этом сам термин «резус-фактор» употребляют лишь по отношению к наиболее иммуногенному (то есть потенциально более способному вызывать иммунный ответ) антигену D. Он играет роль ключевого компонента не только при переливании крови, но и в период беременности, в определенных ситуациях вызывая резус-конфликт.
Как правило, положительный резус-фактор обозначают «Rh+» (при наличии в эритроцитах антигена D), а отрицательный — «Rh–» (при отсутствии антигена D). Резус-положительными являются около 85% европейцев, тогда как остальные 15% имеют «Rh–».
Когда возникает резус-конфликт?
Резус-фактор наследуется как простая менделевская доминанта независимо от системы «АВ0». Это означает, что у резус-положительных родителей в 100% случаев будет резус-положительный ребенок, если они оба гомозиготны (DD), и 25% вероятность того, что малыш будет иметь «Rh–», если они гетерозиготны (Dd).
Важно знать, что так называемый резус-конфликт развивается только в ситуации, когда у будущей мамы отрицательный резус-фактор, а у биологического отца ребенка —положительный.
Резус-конфликт — это несовместимость между кровью резус-отрицательной (Rh–) матери и резус-положительного (Rh+) плода. В его основе лежит иммунный ответ организма женщины на антигены эритроцитов плода. При этом образуются антитела — белки-иммуноглобулины, призванные защищать организм от агентов с признаками генетической чужеродности. Антитела вызывают гемолиз (разрушение) эритроцитов, следствием чего является гемолитическая болезнь плода (ГБП) и гемолитическая болезнь новорожденного (ГБН). Среди клинических форм ГБН выделяют желтушную, анемичную, отечную и смешанную. При желтушной форме в результате разрушения эритроцитов повышается уровень биллирубина, что может привести к поражению клеток головного мозга, судорогам, глухоте, церебральному параличу и задержке умственного развития ребенка.
Проявлениями наиболее тяжелых форм ГБП и ГБН являются асцит (скопление свободной жидкости в брюшной полости), анемия, плевральный выпот [3].
Принято считать, что резус-конфликт не развивается при первой беременности. В то же время иммунизация женщины резус-антигеном может произойти еще до наступления беременности (к примеру, при переливании крови, во время сексуальных контактов), а также в результате проблем с плацентой в период самой беременности.
К тому же некоторое количество беременностей заканчивается самопроизвольным выкидышем на доклинических стадиях (до установления задержки очередной менструации и положительного теста на беременность). Таким образом, первая беременность может быть уже не первой, но женщина даже не подозревает об этом.
Диагностика и профилактика резус-конфликта
Согласно Приказу МЗ Украины № 417 (2011 г.) при угрозе резус-конфликта (если беременная Rh–, а отец ребенка Rh+) содержание анти-D-антител определяют во время первого посещения женской консультации, а также в 28 нед беременности [4].
В соответствии с Практическими рекомендациями Британского Королевского колледжа акушеров-гинекологов (RCOG, 2014 г.) показано проведение неинвазивного ультразвукового допплеровского мониторинга анемии плода по среднемозговой артерии параллельно с определением генотипа плода по его ДНК в образцах материнской крови. Определять группу крови, Rh-фактор и наличие анти-D-антител у резус-отрицательных пациенток следует на 8–12-й неделе беременности. Помимо этого на 28-й неделе рекомендовано дополнительное повторное определение группы крови и резус-фактора [3].
Читайте также: 2017 – год важных достижений в сфере редактирования генома
Для профилактики резус-конфликта беременной вводят антирезусный иммуноглобулин. Делать это нужно до того как произошла сенсибилизация, то есть пока в крови будущей мамы не появились антитела — их отсутствие является обязательным условием для проведения профилактики. Как правило, антирезусный иммуноглобулин в дозе 250 мкг вводят внутримышечно на 28–32-й неделе беременности, а также повторно в послеродовой период [5].
Следует отметить, что некоторые аллели гена RhD эволюционировали с помощью геномных точечных мутаций и рекомбинаций, следствием чего стало появление промежуточных состояний (так называемый серологически слабый D-фенотип — «weak D»). В результате у таких людей часто возможны ложные результаты иммунологических анализов. Кроме того, в период беременности резус-отрицательным женщинам также нецелесообразно назначать иммуноглобулин [6, 7].
Подготовила Александра Демецкая, канд. биол. наук
Литература
- Githiomi R, Waiganjo N., Muna K. The heterogeneity and distribution patterns of AB0 and RhD phenotypes in the voluntary bloodd on ors of Kenya // Аcademic journals 2017; 8 (1): 1-7.
- Landsteiner K., Wiener A. STUDIES ON AN AGGLUTINOGEN (Rh) IN HUMAN BLOOD REACTING WITH ANTI-RHESUS SERA AND WITH HUMAN ISOANTIBODIES // JEM Home 1941 74 (4): 309.
- Демченко О.Б. Современные аспекты проблемы гемолитической болезни плода и новорожденного (Клиническая лекция) // Здоров’я України. – 2017. – № 2 (26).
- Наказ МОЗ України від 15.07.2011 № 417 «Про організацію амбулаторної акушерсько-гінекологічної допомоги в Україні»
- Гемолітична хвороба плода і новонародженого. Клінічний протокол / Додаток до наказу МОЗ № 255 від 27-04-2006.
- Sandler SG et al. Policies and procedures related to testing for weak D phenotypes and administration of Rh immunоglobulin: results and recommendations related to supplemental questions in the Comprehensive Transfusion Medicinesurvey of the College of American Pathologists // Arch Pathol Lab Med. 2014 May; 138 (5): 620-5.
- Haimila K. et al. Targetedantenatal anti-D prophylaxis program for RhD-negative pregnant women – outcome of the first two years of a national program in Finland // Acta Obstet Gynecol Scand. 2017 Oct; 96 (10): 1228-1233.
“Фармацевт Практик” #2′ 2018


