Тетяна Думенко: чому і як змінюється співпраця держави й фармвиробників
Як змінюється співпраця держави й фармвиробників, і що це означає для пацієнта, розповідає Тетяна Думенко, директор Державного Експертного Центру МОЗ України:
Ми всі час від часу купуємо ліки і читаємо до них інструкцію. Державний експертний центр є саме тією установою, яка перевіряє, щоб кожен рядок інструкції мав відповідне підтвердження.
Загалом вся робота ДЕЦ направлена на те, щоб надати пацієнтам України доступ до сучасних та ефективних ліків, що пройшли клінічні випробування та відповідають належним вимогам якості й безпеки.
Водночас ДЕЦ є тією установою, яка першою контактує з виробником ліків або його представником, який хоче або провести клінічне дослідження, або зареєструвати новий лікарський засіб. Саме за рекомендаціями ДЕЦ Міністерство охорони здоров’я приймає рішення про те, щоб зареєструвати ліки в Україні, і вони потрапили до пацієнтів.
Гарантія якості та безпеки препаратів, які схвалюються для застосування в Україні, забезпечується великою кількістю процедур. Тому експертиза одного лікарського засобу триває до 210 днів. Із документами одного заявника працюють від трьох до шести різних експертів, кожен з яких може подавати свої зауваження та запитувати додаткову інформацію у заявника, і багато з цих процесів можуть відбуватися лише послідовно.
Адже у першу чергу, як експертна установа ДЕЦ має забезпечити належну перевірку препаратів, щоб на український ринок потрапили тільки якісні, безпечні та ефективні ліки. З іншого боку, розглядати заявки від виробників треба у найкоротший можливий термін, щоб нові ліки потрапляли українським пацієнтам без затримок.
Тому восени 2016 р. вже вступила в силу спрощена процедура державної реєстрації лікарських засобів. За нею ліки, які вже зареєстровані у США, Швейцарії, Японії, Австралії, Канаді та ЄС,розглядаються в ДЕЦ у найкоротші терміни.
За спрощеною процедурою в Україні вже зареєстровано 110 препаратів. Розгляд за нею триває у середньому 7-10 днів.
Проте, для того, щоб робити зміни в системі охорони здоров’я, орієнтовані на людину, просто скорочувати процедури недостатньо. Тим більше, що скорочувати терміни розгляду без втрати якості експертизи можна лише в окремих випадках. Тому ми прагнемо кардинально змінити підхід до взаємодії між виробниками ліків і державою. Щоби ця взаємодія відбувалась у максимально прозорий спосіб, на рівних для всіх виробників і зручних умовах.
Перш за все, ми запровадили низку електронних послуг: це подання заявок на реєстрацію, перереєстрацію, продовження реєстрації ліків. Усі заявники мають відкритий доступ до інформації про те, на якій стадії перебуває розгляд їхніх документів. ДЕЦ регулярно обмінюється інформацією із кожним заявником через онлайн-кабінет.
Наступним кроком у березні 2019 р. ми відкрили Сервісний центр ДЕЦ. Через нього вже надаються усі послуги для заявників ДЕЦ та «Єдиного вікна» МОЗ: прийом документів, видача готових документів, консультації експертів ДЕЦ.
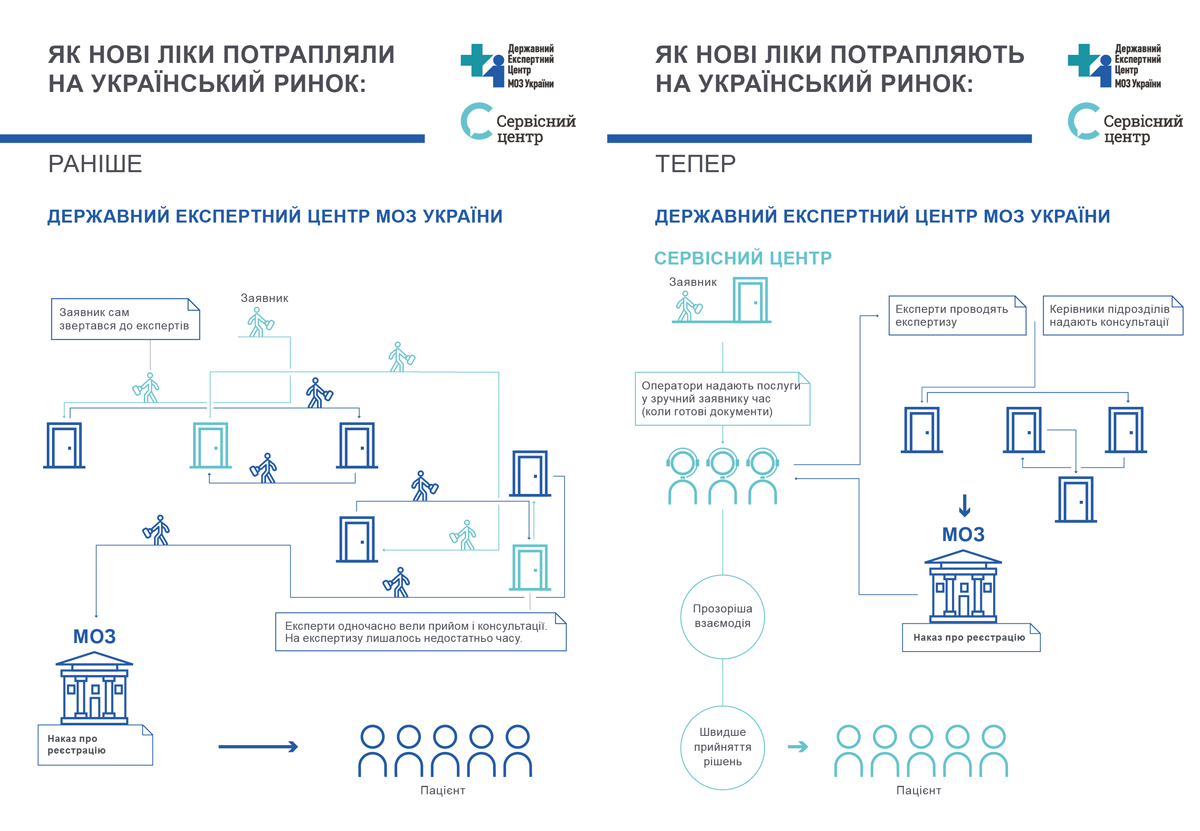
Що це змінить у взаємодії з заявниками, показано на інфографіці нижче. Наведу лише два приклади разючих змін:
- Раніше заявник міг чекати своєї черги на подання документів до двох тижнів. Зараз же він може звернутися до Сервісного центру, як тільки зібрав повний пакет документів.
- Кожен з експертів ДЕЦ отримав додатково 45 годин на місяць для своєї основної роботи – проведення експертизи. Адже експерти звільнилися від обов’язку приймати документи в заявників – цим тепер займаються оператори.
Лише за перший тиждень роботи через Сервісний центр ми вже прийняли 1200 документів до ДЕЦ та 530 заяв до «Єдиного вікна» МОЗ. Це – усі документи, що були заплановані на цей тиждень, а також реєстраційні досьє, що стояли у черзі на наступні два тижні.
Відкриття Сервісного центру державної експертної установи – це поки що унікальний досвід для України. Але це стандартна практика для аналогічних структур у європейських країнах
Сервісний центр є першою точкою контакту для багатьох іноземних виробників ліків з українським ринком. А отже, від якості взаємодії на цьому етапі значною мірою залежить, чи захоче компанія далі інвестувати в Україну та працювати на нашому ринку. А це означає доступ до сучасного лікування для тих, хто найбільше цього потребує, українських пацієнтів.
Джерело: ДЕЦ


