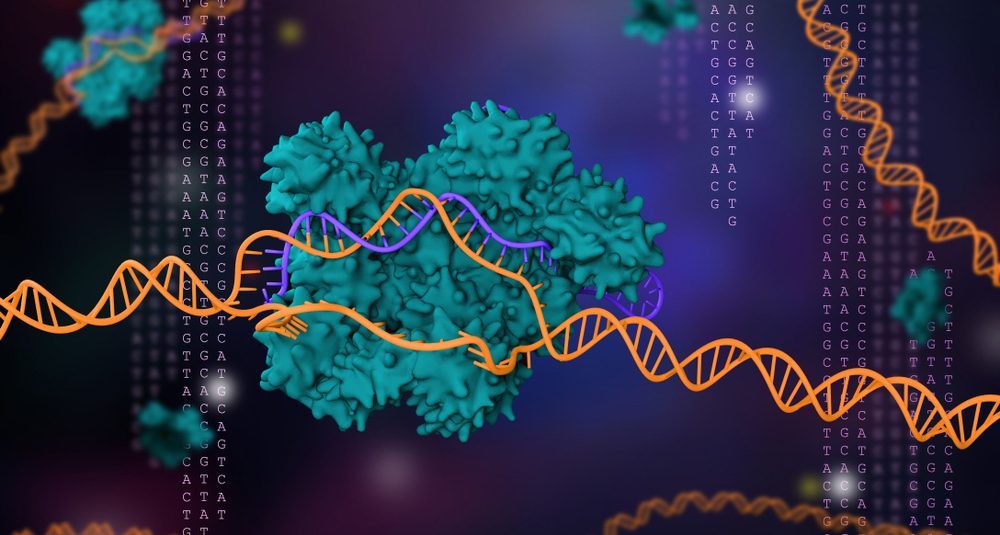
Технології майбутнього: система бактеріального імунітету CRISPR
Історія редагування геному людини починається з дослідження бактерій. Вони, як і людина, схильні до зараження вірусами (бактеріофагами або просто фагами). Приблизно в 50-х роках минулого століття вчені виявили, що одні види бактерій заражаються фагами повільніше, ніж інші, але з часом віруси адаптувалися, і вся колонія втрачала резистентність до вірусу. Це явище пояснюється високою швидкістю вірусних мутацій. Після низки мутацій імунітет бактерії не впізнає вірус, і фаг вільно поширюється колонією. У 2007 р. було виявлено, що певні послідовності нуклеотидів у геномі бактерій пов’язані із набуттям імунітету. За даними подальших досліджень були визначені не тільки механізми формування бактеріального імунітету в ході еволюції та різноманітність його молекулярних інструментів, а й те, як саме його можна використовувати на практиці
Загадкові фрагменти
Наприкінці 80-х років минулого століття з’явилися перші повідомлення про наявність в геномах бактерій (кишкової та туберкульозної паличок, а також деяких ціанобактерій і архей — одноклітинні мікроорганізми, які не мають ядра) серій паліндромних повторів (повторюваних послідовностей ДНК) з короткими вставками між ними. Що це за повтори та навіщо вони потрібні, було не зовсім зрозуміло, спочатку їх сприймали лише як перешкоду при складанні фрагментів геномів. У 90-х роках виявилося, що повтори — це не «екзотичний» елемент ДНК окремих бактерій, а вельми поширений компонент їхніх геномів. У 2002 р. ці повтори отримали назву CRISPR, поблизу яких були виявлені гени cas, що кодують білки — ферменти-ендонуклеази, які розрізають ДНК.
За цим слідували роботи наукової групи однієї з промислових харчових компаній, яка, зокрема, займалася бактеріями для виготовлення молочнокислих продуктів. З цією метою використовували послідовності CRISPR для розрізнення штамів бактерій Streptococcus thermophilus, які застосовують при виготовленні йогуртів. У ході досліджень було встановлено, що отримані кластери паліндромних повторів співвідносяться зі стійкістю до вірусних інфекцій.
Що таке система CRISPR?
Встановлено, що CRISPR — це своєрідна база даних бактерії про контакти із вірусами, подібна до того, як лімфоцити людини зберігають інформацію про контакти з інфекційними агентами, забезпечуючи швидку відповідь імунної системи на потрапляння в організм бактерій або вірусів, з якими людина вже зустрічалася. Механізм роботи бактеріального імунітету зводиться до такого: якщо бактерії вдавалося перемогти вірус, вона вбудовувала фрагменти його ДНК у власний геном, формуючи свого роду картотеку вірусів, з якими стикалася раніше.
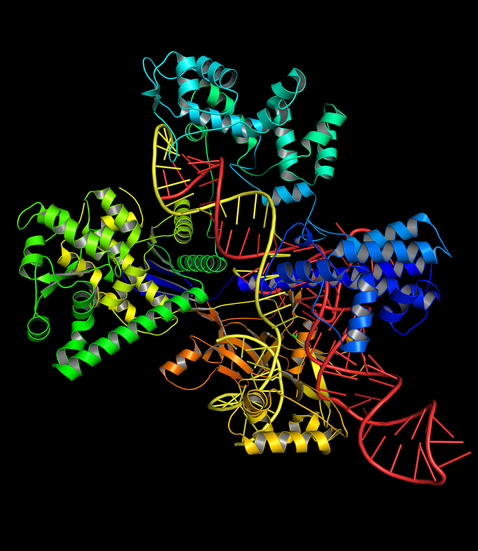
Комплекс CRISPR/Cas та ДНК
В ході подальших експериментів було доведено роль системи CRISPR/Cas у забезпеченні адаптивного імунітету бактерій [1].
Вся система покликана впізнати чужорідну нуклеотидну послідовність і закріпитися на ній. Після цього в хід йдуть нуклеазні ножиці (ендонуклеази, що входять в Cas) або інші засоби (наприклад, РНКази), які розрізають вірусну ДНК. Ворога, таким чином, знешкоджено, а «шматочок» його ДНК буде вставлено в бактеріальний геном та передано нащадкам бактерії. Саме в такий спосіб у бактерій формується набутий імунітет. Він постійно оновлюється у міру контакту бактеріальної клітини із вірусними інфекціями [2].
Згодом на підставі системи бактеріального імунітету CRISPR було розроблено технологію з однойменною назвою, яка дозволяє «переписувати» дефектну ДНК, замінюючи пошкоджені гени на здорові. «CRISPR-лихоманка» охопила науковий світ, і з того часу кількість «заражених» тільки збільшується. Але технології, що здатна змінити світ, доводиться переживати патентні, етичні та законодавчі перипетії.
Спроби та перешкоди
Вчені виявили здатність системи CRISPR/Cas функціонувати не тільки в бактеріальних клітинах, а й в клітинах людини, що дало чергову надію фахівцям у сфері генетичної інженерії та генної терапії. Особливості одночасної взаємодії двох різнорідних нуклеїнових кислот (ДНК та РНК), а також білка дозволили вченим заміняти білки в складі комплексу Cas і проводити не тільки розрізання ДНК, але й «витягування» з неї фрагментів та навіть їхню заміну.
В ідеалі, генну терапію необхідно проводити на ранньому етапі розвитку людського організму. Наслідуваний генний дефект наявний вже на етапі зиготи — коли майбутня людина представлена декількома майже ідентичними клітинами.
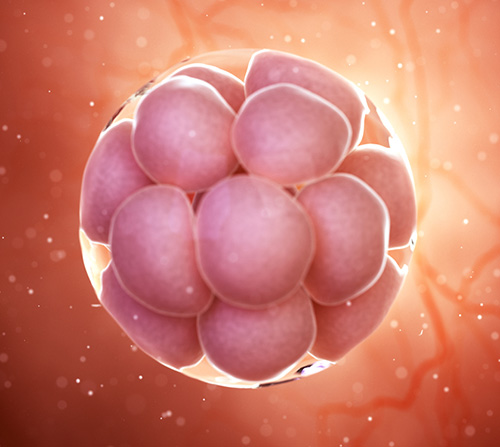
Людський ембріон на стадії 16 клітин, 3D-модель
Припустимо, що у нас є людська зигота із генним дефектом ферменту, відповідального за метаболізм галактози в крові. Дефект гена і, як наслідок, дефект ферменту спричиняє накопичення спирту галактіолу, надлишок якого негативно діє на нервову систему, а також зумовлює розвиток катаракти. Вченим вже відома послідовність нуклеотидів, притаманна «правильному» гену. Залишається тільки зібрати правильний ген, приєднати до нього гени, що кодують систему Cas, і впровадити їх у клітину. В результаті із зиготи має розвинутись організм без будь-яких ознак порушення метаболізму галактози.
У 2012 р. були проведені перші експерименти з модифікації геному за допомогою системи CRISPR/Cas9 [3]. Відсоток помилок в перших експериментах був дуже високий, а самі вони не були визнані «чистими». Однак поступово кількість помилок зменшилась. Перші досліди вчені ставили на рослинних культурах, пізніше перейшли на тварин. У 2013 р. з’явилися перші повідомлення про редагування геному стовбурових клітин людини, хворої на муковісцидоз — захворювання, що порушує функцію залоз зовнішньої секреції і спричиняє закупорку їхнього просвіту в підшлунковій залозі, кишкових залозах, залозах трахеобронхіального дерева та іншіх). Було висловлено припущення, що виправлені клітини можна підсадити людині й тим самим «прищепити» нормальний ген усім клітинам організму.
Читайте також: Революция в редактировании генома
У квітні 2015 р. експеримент китайських вчених (в цій країні етичні норми для біомедичних досліджень є менш суворими, ніж у західних країнах) на людських ембріонах продемонстрував, що, на жаль, метод потребує вдосконалення [4]. Справа в тому, що замінити гени вдалося тільки у 4 випадках з понад 50. При цьому система CRISPR/Cas9 не лише змінила гени, які планувалося замінити, але й внесла інші, незаплановані та небажані корективи.
Перспективи
У грудні 2015 р. вчені Массачусетського університету (США) представили результати нової роботи із CRISPR/Cas9 [5]. Модифікувавши код СAS, вони різко підвищили точність роботи системи, що майже повністю виключає ймовірність помилок.
Якщо не вдаватися в технічні подробиці, сьогодні CRISPR/Cas9 дозволяє легко, дешево і швидко переміщувати будь-які гени до будь-яких живих істот, від бактерій до людини, що дійсно є вирішальним моментом в історії біомедичних досліджень.
З’явилися стартапи, присвячені CRISPR. Міжнародні фармацевтичні та сільськогосподарські компанії поступово переключаються на розробку технологій на основі CRISPR. Використовуючи цю технологію, вченим вже вдалося виправити деякі мутації, що призводять до сліпоти, та зупинити поділ ракових клітин [6]. Агрономи отримали пшеницю, невразливу для грибкових захворювань (таких як борошниста роса). Отже, в перспективі такі вдосконалені сільськогосподарські культури зможуть прогодувати 9 млрд людей на планеті, де стрімко теплішає. Біоінженери використали CRISPR, щоб змінити ДНК дріжджів, то ж відтепер дріжджі можуть споживати рослинну біомасу і виділяти етанол — технологія обіцяє кінець залежності від нафтохімії.
Для багатьох вчених CRISPR — це сяючий світ майбутнього, Нобелівські премії та значні прибутки. Але варто пам’ятати про те, що це революційна технологія, і, як будь-яка революція, вона може призвести до непередбачуваних наслідків. Теоретично вона може нарешті дозволити вченим як за помахом чарівної палички здійснити все те, чим генетика так лякає обивателів: створених на замовлення немовлят, мутантів, які витісняють звичні види, видоспецифічну біологічну зброю й десятки інших «апокаліптичних» винаходів із наукової фантастики. Нова технологія повністю змінює правила гри в галузі біомедичних досліджень. При цьому ніхто не знає, якими будуть ці правила, і хто першим наважиться їх порушити…
Читайте також: Что такое эндогенные ретровирусы, и что они делают в геноме человека?
Підготувала Олександра Демецька, канд. біол. наук
Література
- Barrangou R. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. — 2007 Mar 23; 315 (5819): 1709–12.
- Al-Attar S. еt al. Clustered regularly interspaced short palindromic repeats (CRISPRs): the hallmark of an ingenious antiviral defense mechanism in prokaryotes // Biol Chem. — 2011 Apr; 392 (4): 277–89.
- Giedrius Gasiunas et al. Cas9–crRNA ribonucleoprotein complex mediates specific DNA cleavage for adaptive immunity in bacteria. PNAS September 25;2012.109(39):15539-15540.
Xiao-Jie L. еt al. CRISPR-Cas9: a new and promising playеr in gene therapy // J Med Genet. — 2015 May; 52 (5): 289–96. - Doudna J. Genome-editing revolution: my whirl wind year with CRISPR // Nature. — 2015; 22 December.
- Hinze L. et al. Synthetic Lethality of Wnt Pathway Activation and Asparaginase in Drug-Resistant Acute Leukemias // Cancer Cell. — 2019 Apr 15; 35 (4): 664–676.
“Фармацевт Практик” #6′ 2019