ДЕЦ презентував зміни у процедурі реєстрації лікарських засобів
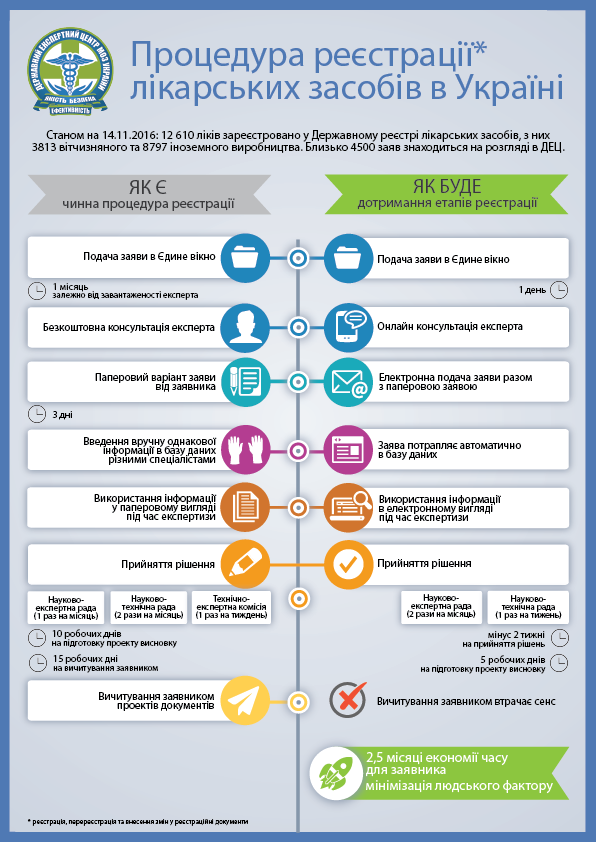
Державний експертний центр (ДЕЦ) презентував зміни у процедурі реєстрації, перереєстрації та внесення змін у реєстраційні документи лікарських засобів, завдяки яким вона проходитиме швидше для заявників. Такі зміни очікуються завдяки можливості подачі електронної заяви заявником, яка дозволить мінімізувати людське втручання та уникнути внесення інформації вручну експертами ДЕЦ, а також завдяки зменшенню числа комісій та змінам у регулярності їх засідань. Зокрема буде ліквідована Технічно-експертна комісія, а Наукова експертна рада та Науково-технічна рада виноситимуть рішення двічі на місяць та щотижня, відповідно.
Одночасно з цим ДЕЦ запроваджує зміни, спрямовані на підвищення прозорості установи та усіх процедур. Уже відкритий реєстр клінічних досліджень, які плануються до проведення. А також оприлюднена фінансова звітність діяльності ДЕЦ – її розміщено на веб-сайті Центру. На веб-сайті протягом наступного року можна буде знайти інформацію щодо поданих заяв, етапів реєстрації, звітів експертів, які обґрунтовують прийняте рішення – дозвіл або відхилення реєстрації ліків. Найближчим часом також будуть відкриті й результати проведених в Україні клінічних випробувань. Зокрема у 2016 році в Україні проведено 250 клінічних досліджень: 196 міжнародних та 54 національних.
 Тетяна Думенко, директор Державного експертного центруМіністерства охорони здоров’я
Тетяна Думенко, директор Державного експертного центруМіністерства охорони здоров’я
України: «Завдання, які я ставлю перед собою та командою ДЕЦ на наступний рік, та які ми вже почали втілювати, стосуються двох напрямів: відкритості та прозорості роботи ДЕЦ, а також покращення якості та вчасності надання послуг з реєстрації, перереєстрації та внесення змін в реєстраційні документи. Я хочупідкреслити, що реєстрація ліків – це не бар’єр, а гарантія доступу до якісних, ефективних та безпечних ліків. І ми будемо далі працювати над тим, щоб цей процес був якомога прозорішим, простішим та зрозумілішим для заявників та для пацієнтів».
Низка заходів, спрямованих на покращення якості послуг ДЕЦ, включатиме постійне навчання експертів, підвищення їхньої персональної відповідальності, а також підвищення зарплатні. Крім того, його гарантуватимуть дотримання стандартів управління якістю: у 2017 році планується ресертифікація відповідно до ISO 9001/2015. Задля уникнення ризиків, пов’язаних з конфліктом інтересів та корупцією, усі співробітники ДЕЦ заповнюватимуть електронні декларації щодо конфлікту інтересів експертів.
Роман Ілик, заступник міністра охорони здоров’я України: «Забезпечення доступу пацієнтів до сучасних і якісних ліків – це один з пріоритетів реформи системи охорони здоров’я в Україні. Зміни у роботі ДЕЦ – один з перших і важливих кроків на цьому шляху. Вже у 2017 році істотні результати цих змін побачать як постачальники ліків, так і пацієнти».
Загалом в Україні зареєстровано 12 610 найменувань ліків, з яких українського виробництва – 3 813, іноземних – 8 797. Крім того, у роботі в ДЕЦ на сьогодні знаходиться 4,5 тисяч заявок на реєстрацію, перереєстрацію та внесення змін до реєстраційних документів. Ця інформація розміщена у відкритому доступі на веб-сайті ДЕЦ, її оновлення відбувається щоденно.
Джерело: ДЕЦ
