Есть ли смысл в разработке антисенсов?
Антисмысловые олигонуклеотиды, или антисенсы, названы так потому, что они как бы «отражают смысл» молекул, кодирующих белковые последовательности. Их используют для снижения или повышения уровня экспрессии белков, участвующих в развитии патологии. На разработку лекарственных средств на их основе возлагали большие надежды. Ученые высказывали предположение, что антисенсы помогут в лечении смертельных болезней, но с ними также связаны неудачи и скандалы. Есть ли будущее у этих лекарственных средств?
Что такое антисенсы?
Антисенсы — это класс лекарственных средств, представляющих собой относительно короткие нуклеотидные цепочки, состоящие из 15–40 нуклеотидов. Антисмысловые олигонуклеотиды способны образовывать гибрид с матричной РНК (мРНК) и ингибировать ее нормальную трансляцию на рибосомах.
Нуклеотидная последовательность мРНК несет смысловую информацию об аминокислотной последовательности белка, являющегося продуктом соответствующего гена. Ингибирование, в отличие от выключения гена, обратимо и требует продолжительного присутствия антисенсов. Различные химические модификации антисенсов повышают их стабильность в клетке и усиливают связывание с РНК-мишенью. Это могут быть как немодифицированные РНК и ДНК, так и олигонуклеотиды, содержащие всевозможные модификации самих звеньев или концов цепочки.
В самом простом случае антисенсы связываются с мРНК и блокируют трансляцию белка, не позволяя рибосоме продвигаться по кодирующей цепи. Антисмысловые олигонуклеотиды применяют в онкологии для подавления синтеза опухолевых белков. Антисенсы могут убрать из зрелой мРНК участки, кодирующие мутации, которые вызывают тяжелые заболевания.
Читайте также: Нобелевская премия по химии 2015. ДНК: работа над ошибками
Преимущество антисмысловой технологии, основанной на использовании антисенсов, заключается в том, что она позволяет конструировать специфические ингибиторы экспрессии любого представляющего интерес гена, основываясь лишь на знании его нуклеотидной последовательности.
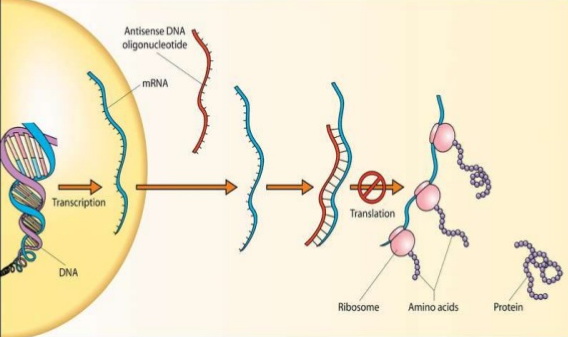
Антисмысловой олигонуклеотид (красный цвет) связывается с матричной РНК (синий цвет) и таким образом препятствует синтезу белка (серый цвет) на рибосомах (розовый цвет)
Несбывшиеся надежды онкологии
Большие надежды на антисенсы возлагали в онкологии. Так, для борьбы с раком легкого, предстательной и молочной железы долгое время в разработке находился custirsen (Oncogenex) — антисенс против белка кластерина. Секреция этого белка значительно усиливается при многих видах рака и проявляется резистентностью к терапии, повышая устойчивость раковых клеток к апоптозу. Результаты первых исследований выглядели весьма обнадеживающе, однако в связи с недостаточной эффективностью последних фаз программу закрыли.
В качестве антисенсов могут выступать как немодифицированные РНК и ДНК, так и олигонуклеотиды, содержащие всевозможные модификации самих звеньев или концов цепочки
Еще один антисенс, используемый в онкологии, трабедерсен (Autotelic) разрабатывали против глиомы, меланомы и рака поджелудочной железы. В этом случае в качестве мишени был выбран цитокин, участвующий во множестве процессов, связанных с воспалением, фиброзом и онкогенезом. Но его роль в значительной степени зависит от конкретного типа клеток, поскольку на ранних стадиях развития опухоли он является ингибитором роста опухоли и онкосупрессором, а на поздних — стимулятором прогрессирования рака. Несмотря на не совсем удачный выбор мишени, третья фаза испытаний при глиомах была остановлена только из-за медленного набора пациентов.
Читайте также: Создан организм с искусственной ДНК, способной к неограниченному делению
История провалов
У антисенсов печальная история провалов. Разработка более 400 молекул остановлена из-за недостаточной эффективности или безопасности. Первый антисенс fomivirsen (Novartis) был зарегистрирован в 1998 г. и предназначался для местного применения (инъекции в глаз) при воспалении сетчатки у пациентов с ВИЧ. Но в связи с многочисленными побочными эффектами и благодаря разработке эффективной антиретровирусной терапии против ВИЧ проблема ретинита отошла на второй план, поэтому препарат отозвали в странах Европы и в США.
Антисмысловая технология, основанная на использовании антисенсов, позволяет конструировать специфические ингибиторы экспрессии любого представляющего интерес гена, основываясь лишь на знании его нуклеотидной последовательности
Следующий антисенс аликафорсен (Atlantic) пытались использовать для лечения тяжелых форм аутоиммунных воспалительных заболеваний — ревматоидного артрита, псориаза и болезни Крона. Однако в фазе ІІІ он оказался недостаточно эффективен в терапии болезни Крона, после чего остальные разработки были также остановлены. Тем не менее сейчас возобновили исследования по язвенному колиту и резервуарному илеиту и есть надежда на положительный результат.
Антисенс aganirsen (GeneSignal) разрабатывали по множеству офтальмологических показаний: диабетической ретинопатии, окклюзии вен сетчатки, диабетическому макулярному отеку, неоваскуляризации роговицы и даже для терапии псориаза. Сейчас разработки остановлены практически по всем направлениям, вероятно, в связи с их неэффективностью, но несмотря на это, компания GeneSignal продолжает исследования.
Скандал в FDA
Eteplirsen (Sarepta) — наиболее скандальный препарат класса антисенсов. Его разрабатывали для лечения миодистрофии Дюшенна. Эта редкая болезнь возникает при дефектах в гене дистрофина — структурного белка мышечных клеток, защищающего мышцы от повреждений, вызванных растягиванием. При этом наступает прогрессирующая мышечная слабость скелетных мышц, которая к 12 годам приводит к глубокой инвалидности. Средняя продолжительность жизни таких больных составляет 20–30 лет.
Читайте также: Как мутирует человечество?
Новый препарат заставлял рибосому пропускать дефектный участок и в результате получался функционирующий белок этеплирсен, который исследовали с участием 12 пациентов. Несмотря на то что было достигнуто увеличение количества функционального дистрофина в мышцах, FDA потребовало предоставить больше данных. Результаты нового исследования показали, что у 13 пациентов средний прирост уровня дистрофина повысился с 0,16 до 0,44% по сравнению с нормальным показателем, причем менее чем у половины участников. Похожие результаты были получены при исследовании антисенса drisapersen (BioMarin), который продемонстрировал повышение уровня дистрофина в мышцах у 12 пациентов. Потом в фазе ІІІ исследования у 300 пациентов статистически значимых различий с плацебо не было обнаружено, поэтому программу закрыли.
В случае с этеплирсеном под давлением общественности препарат все-таки был зарегистрирован FDA вопреки отрицательному заключению экспертов. Но если дальнейшие исследования этеплирсена не продемонстрируют существенных физиологических улучшений, препарат будет отозван. В FDA в связи с этеплирсеном разгорелся нешуточный скандал. Официальные лица в FDA настоятельно рекомендуют другим компаниям не следовать примеру Sarepta и предоставлять только качественные данные для обоснования регистрации своих продуктов.
История успехов — одобрено и не скомпрометировано
Препарат nusinersen (Biogen) — пожалуй, единственный антисенс, получивший одобрение в Европе, США и других странах, и пока не скомпрометировавший себя ни скандалами, ни отказами, ни побочными действиями. Это первый препарат, доказавший свою эффективность при спинальной мышечной атрофии у взрослых и детей. Спинальная атрофия приводит к мышечной атрофии и гибели от дыхательной недостаточности, причем она является причиной большинства детских смертей от врожденных заболеваний. На основании результатов нескольких клинических исследований доказана высокая безопасность и эффективность нового препарата.
Тем не менее специалисты считают, что об успехах в области антисенсов всегда надо говорить с осторожностью. Например, на препарат mipomersen возлагали большие надежды в лечении патологий, связанных с повышенным содержанием липопротеинов низкой плотности в крови, которые являются основными переносчиками холестерина. Их часто называют «плохим холестерином» из-за связи с риском атеросклероза, приводящего к повышению частоты случаев инсульта, инфаркта миокарда и других сердечно-сосудистых осложнений.
Мипомерсен снижает экспрессию одного из основных белков семейства липопротеинов низкой плотности. Как было установлено в клинических исследованиях, мипомерсен действительно снижал уровень липопротеинов в сыворотке крови пациентов, однако при этом значимо повышал риск гепатотоксичности. Поэтому FDA одобрило препарат только для ограниченного использования, а ЕМА (Европейское медицинское агентство) отказало ему в регистрации.
Определенная категория вирусов, называемая ретровирусами, включая ВИЧ, проникает в клетку в виде цепочек РНК и потому служит хорошей мишенью для антисенсов
Есть ли будущее у антисенсов?
В разработке в фазе ІІІ сейчас находится 12 антисенсов, в фазе ІІ — 62. Многие из них предназначены для лечения смертельных заболеваний, и проводимые исследования дают надежды на высокую эффективность и безопасность этих препаратов.
Несмотря на впечатляющую историю провалов, разработка антисенсов определенно имеет смысл. Но справедливости ради следует отметить, что сфера их применения ограничена специальными случаями, то есть редкими заболеваниями, при которых именно манипуляции с мРНК позволяют достичь терапевтического эффекта.
Читайте также: Революция в редактировании генома (часть 1)
Революция в редактировании генома (часть 2)
Накапливается все больше данных о том, как повысить безопасность и эффективность антисенсов. Однако антисмысловым олигонуклеотидам все еще далеко до таких универсальных инструментов терапии, какими стали малые молекулы или антитела. Перспективной целевой мишенью антисенсов являются вирусные и бактериальные инфекции, но пока на завершающих стадиях разработки находится всего несколько антисенсов против гепатитов В и С.
Определенная категория вирусов, называемая ретровирусами, включая ВИЧ, проникает в клетку в виде цепочек РНК и потому служит хорошей мишенью для антисенсов. Во время клинических исследований технологии антисенсов принесли многообещающие результаты и в будущем могут спасти миллионы людей, страдающих от ВИЧ-инфекции. А если есть хотя бы малейший шанс на спасение, его обязательно надо использовать, поэтому у антисенсов есть перспективы.
Татьяна Кривомаз,
д-р техн. наук, канд. биол. наук, профессор
“Фармацевт Практик” #4′ 2018